Pandemias, resistência microbiana e crises globais estão mudando a saúde. Entenda por que prevenção e controle de infecção se tornaram estratégicos para profissionais, gestores e instituições no século XXI.
Resumo executivo
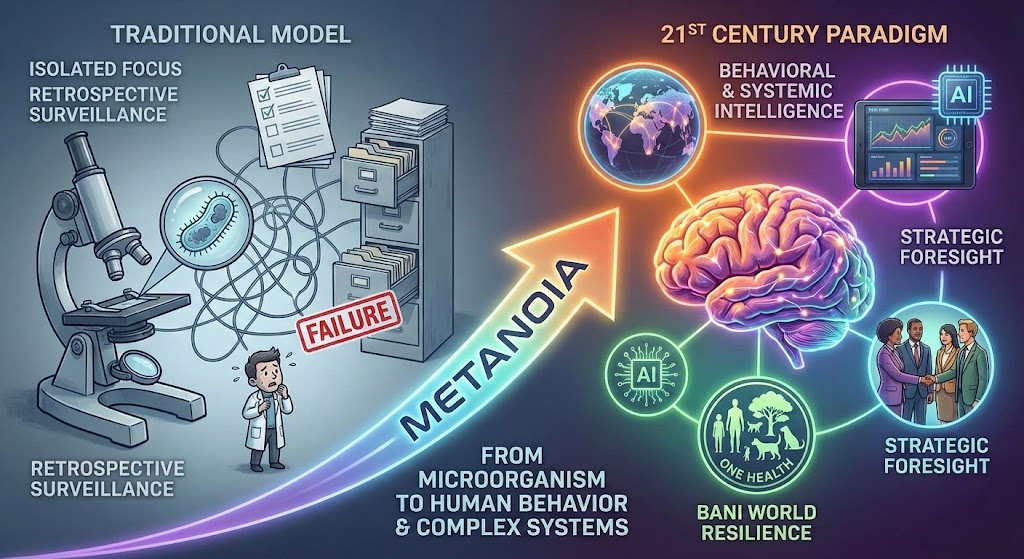
A prevenção e o controle de infecção no século XXI deixaram de ser atividades predominantemente técnicas e normativas para se tornarem eixos estratégicos da segurança do paciente, da sustentabilidade institucional e da inteligência em saúde. Em um contexto marcado pelo fim das certezas lineares e pela dinâmica BANI — frágil, ansiosa, não linear e incompreensível —, modelos centrados apenas em protocolos, vigilância retrospectiva e fiscalização mostram-se insuficientes. O artigo defende uma metanoia profissional e institucional: uma mudança profunda de modelos mentais que reposiciona o controle de infecção do foco exclusivo no microrganismo para a compreensão integrada do comportamento humano, dos sistemas organizacionais e da interdependência entre saúde humana, animal e ambiental. Ao articular fatores humanos, cultura de segurança, liderança, governança, uso inteligente de dados e tecnologias digitais, o controle de infecção passa a atuar como campo-chave de antecipação de riscos, aprendizagem contínua e construção de sistemas de saúde mais resilientes. Nesse novo paradigma, o valor do profissional e das instituições reside menos no cumprimento formal de normas e mais na capacidade de interpretar contextos complexos, integrar evidências e liderar transformações sustentáveis frente aos desafios sanitários do século XXI.
Índice do artigo
- Introdução
- O século XXI e o fim das certezas lineares na saúde
- O mundo BANI e por que a saúde sofre mais
- Metanoia: conceito, sentido e implicações para a prática em saúde
- Do microrganismo ao comportamento: o controle de infecção como campo-chave da metanoia
- Instituições sem metanoia: por que falham mesmo quando “fazem tudo certo”
- A carreira do profissional de saúde no mundo BANI: obsolescência, ansiedade e valor estratégico
- Do microrganismo ao comportamento humano: onde realmente nascem as infecções
- Controle de infecção 4.0: dados, epidemiologia e inteligência artificial na linha de frente
- Integração final: controle de infecção como eixo de inteligência e de futuro em saúde
- Formação, educação e desenvolvimento contínuo: construindo a metanoia na prática
- Liderança, governança e resiliência: o lugar do controle de infecção na alta gestão
- Metanoia em ação: caminhos práticos para transformar o controle de infecção
- Conclusão: o que muda quando a mente muda
FAQ: PREVENÇÃO E CONTROLE DE INFECÇÃO NO SÉCULO XXI
Questão 1: O que define a mudança de papel do controle de infecção no século XXI?
Resposta: A prevenção e o controle de infecção deixaram de ser atividades puramente técnicas e normativas para se tornarem eixos estratégicos da segurança do paciente, da sustentabilidade institucional e da inteligência em saúde. O foco agora está na antecipação de riscos e na capacidade de interpretar contextos complexos.
Referência: https://www.who.int/publications/i/item/9789240051164
Questão 2: Como o conceito de mundo BANI se aplica à saúde atual?
Resposta: O cenário atual é definido como frágil, ansioso, não linear e incompreensível. Na saúde, isso se manifesta em sistemas operando no limite, onde pequenas falhas geram crises desproporcionais e a vigilância tradicional já não consegue prever todos os eventos.
Questão 3: O que é a metanoia profissional e institucional proposta no artigo?
Resposta: Trata-se de uma transformação profunda no modo de pensar e interpretar a realidade. Ela propõe que o profissional e a instituição abandonem o foco exclusivo no microrganismo para adotar uma visão que considere o comportamento humano e os sistemas complexos.
Referência: https://www.ccih.med.br/metanoia-o-que-muda-quando-a-mente-muda/
Questão 4: Por que o foco do controle de infecção deve mudar do microrganismo para o comportamento humano?
Resposta: As infecções raramente ocorrem apenas pela presença de patógenos. Elas emergem de decisões humanas sob pressão, falhas de comunicação e culturas organizacionais que normalizam desvios. O comportamento humano é o principal vetor de risco e a maior oportunidade de mudança.
Referência: https://doi.org/10.1136/bmj.320.7237.768
Questão 5: Qual a relação entre o controle de infecção e o conceito de Saúde Única ou One Health?
Resposta: O conceito reconhece que a saúde humana está ligada à saúde animal e ambiental. O controle de infecção deve entender que riscos como a resistência antimicrobiana nascem de interações globais que envolvem agricultura, pecuária e mudanças climáticas.
Referência: https://www.fao.org/one-health/en
Questão 6: O que caracteriza o Controle de Infecção 4.0?
Resposta: É o uso intensivo de dados, epidemiologia digital e inteligência artificial para antecipar riscos e surtos em tempo quase real. Ele substitui a vigilância manual e retrospectiva por uma análise preditiva que apoia decisões imediatas.
Questão 7: Como a inteligência artificial pode auxiliar as comissões de controle de infecção na prática?
Resposta: A inteligência artificial pode prever riscos de infecção de sítio cirúrgico, identificar precocemente surtos através de padrões ocultos em grandes volumes de dados e apoiar o gerenciamento racional de antimicrobianos.
Referência: https://pmc.ncbi.nlm.nih.gov/articles/PMC12722576/
Questão 8: Por que algumas instituições falham mesmo quando cumprem todos os protocolos técnicos?
Resposta: Isso ocorre pela ausência de metanoia institucional, onde a segurança é reduzida ao cumprimento formal de normas no papel, enquanto a prática real ignora as pressões sistêmicas e os comportamentos que geram riscos invisíveis.
Referência: https://www.who.int/publications/i/item/WHO-HIS-SDS-2016.8
Questão 9: Qual o impacto da ansiedade profissional no contexto do mundo BANI?
Resposta: A ansiedade crônica afeta a qualidade das decisões e favorece comportamentos defensivos. Profissionais pressionados tendem a aderir mecanicamente às normas sem compreender profundamente os processos, o que aumenta a vulnerabilidade do sistema.
Referência: https://www.youtube.com/@CCIHCursosMBA
Questão 10: Como a alta gestão hospitalar pode fortalecer o controle de infecção estrategicamente?
Resposta: A liderança deve posicionar o controle de infecção como parceiro estratégico da gestão, garantindo autonomia técnica e participação em decisões sobre dimensionamento de pessoal, infraestrutura e investimentos em tecnologias.
Referência: https://pubmed.ncbi.nlm.nih.gov/20836582/
Questão 11: O que é o conceito de Just Culture ou cultura justa na saúde?
Resposta: É um modelo onde o erro é tratado como oportunidade de aprendizado sistêmico e não como falha moral individual. Isso estimula o relato aberto de incidentes e permite identificar as condições do sistema que favoreceram o erro.
Referência: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3776518/
Questão 12: Qual a diferença entre trabalho prescrito e trabalho real?
Resposta: O trabalho prescrito é o que está nos protocolos e manuais. O trabalho real é o que acontece na prática sob pressão de tempo e falta de recursos. As infecções frequentemente nascem na lacuna entre esses dois mundos.
Referência: https://www.ccih.med.br/trabalho-prescrito-vs-trabalho-real/
Questão 13: Como enfrentar a resistência microbiana sob a ótica da complexidade?
Resposta: A resistência não se resolve apenas com novos antibióticos. Exige a compreensão de padrões de uso em humanos e animais, pressões institucionais e impactos ambientais, requerendo uma abordagem integrada de gerenciamento.
Referência: https://www.who.int/publications/i/item/9789241509763
Questão 14: Como as mudanças climáticas impactam o controle de infecção hospitalar?
Resposta: Eventos climáticos extremos e desastres ambientais comprometem o saneamento e sobrecarregam os serviços, gerando surtos abruptos que exigem do profissional uma capacidade de leitura sistêmica e respostas rápidas.
Referência: https://doi.org/10.1016/S2542-5196(21)00002-5
Questão 15: O que define um aprendizado transformador para o profissional de saúde?
Resposta: É o processo que cria espaços para problematizar o cotidiano e questionar as premissas que sustentam a prática. Vai além da transmissão de conteúdo, gerando mudanças reais de mentalidade e identidade profissional.
Referência: https://www.normfriesen.info/files/Mezirows_overview_transformative.pdf
Questão 16: Qual a importância da resiliência organizacional na prevenção de infecções?
Resposta: Refere-se à capacidade da instituição de absorver choques e se adaptar mantendo a segurança. O controle de infecção atua como um sensor que identifica vulnerabilidades antes que o sistema colapse diante de uma crise.
Referência: https://pmc.ncbi.nlm.nih.gov/articles/PMC10113996/
Questão 17: O que é a aprendizagem de circuito duplo ou double loop learning?
Resposta: É o aprendizado que não apenas corrige o erro imediato, mas revisa as premissas e as normas de gestão que permitiram que o erro ocorresse, evitando a repetição cíclica de eventos adversos.
Referência: https://theisrm.org/documents/Argyris%20(1977)%20Double%20Loop%20Learning%20in%20Organizations.pdf
Questão 18: Como os dados podem ser transformados em inteligência sanitária estratégica?
Resposta: Através da integração de informações de prontuários, laboratórios e comportamento, permitindo prever tendências e apoiar decisões estratégicas da gestão com base na realidade em tempo real.
Referência: https://www.ccih.med.br
Questão 19: Por que a vigilância retrospectiva isolada se tornou insuficiente no século XXI?
Resposta: Em um mundo de mudanças rápidas e alta interdependência, reagir apenas a eventos já consolidados significa chegar sempre atrasado aos riscos. É preciso antecipar ameaças através de modelos prospectivos.
Referência: https://www.who.int/publications/i/item/WHO-HIS-SDS-2016.8
Questão 20: O que muda na trajetória de carreira do profissional ao adotar essa nova visão?
Resposta: O profissional deixa de ser um fiscal de processos e passa a ser um agente de inteligência e mudança cultural. Seu valor estratégico cresce à medida que ele cria sentido e segurança em meio à incerteza.
Referência: https://www.linkedin.com/in/mba-gest%C3%A3o-ccih-a-tadeu-fernandes-11275529/
Introdução
Nas primeiras décadas do século XXI, a prevenção e o controle de infecções deixaram de ser um campo restrito a protocolos técnicos e rotinas institucionais para se tornar um eixo estratégico da segurança do paciente, da sustentabilidade dos serviços de saúde e da própria trajetória profissional de quem atua nessa área (WHO, 2022). Pandemias recentes, a aceleração da resistência microbiana, a intensificação da mobilidade global e o impacto crescente de eventos climáticos extremos tornaram evidente que o modelo tradicional, centrado na aplicação de normas e na vigilância retrospectiva de microrganismos, tornou-se insuficiente para responder à complexidade atual (LAXMINARAYAN et al., 2013; FAO et al., 2025)
Durante muito tempo, acreditou-se que bastaria cumprir rigorosamente diretrizes, manter comissões formalmente constituídas e controlar indicadores para garantir proteção adequada aos pacientes, profissionais e instituições (WHO, 2016). Essa lógica funcionou razoavelmente bem em um contexto em que os problemas eram mais previsíveis, relativamente estáveis e predominantemente confinados ao ambiente hospitalar. Hoje, no entanto, a saúde opera em um cenário de interdependência global, velocidade inédita de propagação de crises, sobrecarga crônica dos sistemas e pressão intensa sobre decisões clínicas, gerenciais e políticas, como ficou evidente na pandemia de COVID-19 e nas avaliações recentes de capacidade de prevenção e controle de infecções em diferentes países (WHO, 2022).
Nesse novo ambiente, a prevenção e o controle de infecção deixaram de ser apenas exigência regulatória ou atividade operacional para se constituir em componente central da inteligência sanitária, articulando microbiologia, comportamento humano, gestão de risco, Saúde Única, uso de dados e tecnologias digitais, sustentabilidade e governança em saúde (WHO, 2022; FAO et al., 2025). O campo deixa de se limitar à pergunta “quais microrganismos estão envolvidos?” para incorporar questões como “quais decisões, comportamentos e contextos tornaram essa infecção possível?” e “como estruturas institucionais e políticas moldam, sustentam ou reduzem o risco?”, em consonância com abordagens contemporâneas de sistemas complexos e segurança do paciente (PLSEK; GREENHALGH, 2001; BRAITHWAITE et al., 2018
Essa mudança de foco exige um reposicionamento profundo do papel do profissional e da instituição. O perfil centrado exclusivamente na fiscalização de processos e no cumprimento de normas perde relevância em sistemas complexos, marcados por fragilidade, ansiedade, não linearidade e dificuldade crescente de compreensão do todo, enquanto ganha espaço o profissional capaz de ler contextos, articular diferentes áreas, integrar evidências microbiológicas com fatores humanos e organizacionais e atuar de forma estratégica na construção de ambientes mais seguros e resilientes (REASON, 2000; SINGER; VOGUS, 2013
Ao mesmo tempo, instituições que continuam tratando o controle de infecção como um setor periférico, burocrático ou meramente técnico expõem-se a riscos assistenciais, reputacionais, financeiros e regulatórios cada vez maiores, especialmente em países que vêm incorporando avaliações nacionais de programas de prevenção e controle de infecções e de gerenciamento de antimicrobianos (ANVISA, 2024; WHO, 2022). Em um mundo em que crises sanitárias podem se tornar rapidamente crises sociais, econômicas e políticas, pensar prevenção e controle de infecção de forma estratégica deixa de ser diferencial competitivo e passa a ser condição de sobrevivência institucional (WHO, 2022; KICKBUSCH; LEUNG; BHATIA, 2021
Por isso, o grande desafio contemporâneo já não é apenas atualizar protocolos ou incorporar novas tecnologias, mas repensar a forma como se compreende e se pratica o controle de infecção. Trata-se de uma mudança de mentalidade: deslocar o centro da discussão do microrganismo para o comportamento humano e para os sistemas que o moldam, reconhecer a interdependência entre saúde humana, animal e ambiental, e aceitar que segurança duradoura depende da capacidade de aprender continuamente em meio à incerteza, como enfatizam as abordagens de Saúde Única e de sistemas resilientes em saúde (WHO, 2015; FAO et al., 2025; BRAITHWAITE et al., 2018). É a partir desse enquadramento que os capítulos seguintes discutem o fim das certezas lineares na saúde, o impacto do mundo BANI, a necessidade de metanoia profissional e institucional e o reposicionamento do controle de infecção como campo-chave para enfrentar os desafios do século XXI
Capítulo 1 – O século XXI e o fim das certezas lineares na saúde
Durante grande parte do século XX, a organização da saúde foi sustentada por um conjunto relativamente estável de pressupostos que associavam problemas bem definidos a soluções técnicas claramente delineadas. Presumia-se que causas delimitadas conduziriam a efeitos previsíveis e que o domínio da tecnologia, das normas e da especialização profissional seria suficiente para garantir controle, segurança e progresso contínuo. Essa visão linear orientou a formação em saúde, o desenho de protocolos, a estruturação das instituições e a própria identidade dos especialistas.
Esse paradigma produziu avanços inegáveis, especialmente com o desenvolvimento de antimicrobianos, vacinas, métodos diagnósticos e sistemas de vigilância capazes de reduzir mortalidade, controlar surtos e expandir a expectativa de vida. Ao mesmo tempo, consolidou-se uma confiança excessiva na capacidade de domesticar a complexidade sanitária por meio da combinação entre ciência biomédica, prescrição normativa e gestão centrada em desempenho técnico, como se bastasse aprimorar continuamente protocolos e tecnologias para manter riscos sob controle.
O século XXI rompeu de forma contundente com essa expectativa. A saúde passou a operar em um ambiente marcado por interdependência global, aceleração de eventos, múltiplas camadas de risco e interações que escapam à lógica de causa e efeito simples, características típicas de sistemas complexos adaptativos (PLSEK; GREENHALGH, 2001; BRAITHWAITE et al., 2018). Nesse novo contexto, decisões corretas em um ponto do sistema podem gerar consequências inesperadas em outro; pequenas falhas podem desencadear crises amplas; soluções eficazes em determinado momento podem tornar-se rapidamente obsoletas à medida que o contexto se transforma.
Essa ruptura não é exclusiva da saúde, mas nela se manifesta com particular intensidade, justamente porque sistemas de saúde reúnem pessoas, tecnologias, instituições, fluxos de informação, valores, interesses econômicos e expectativas sociais em interação contínua (BRAITHWAITE et al., 2018). Nesses sistemas, as respostas não são proporcionais às intervenções, os comportamentos não são totalmente previsíveis e mudanças no ambiente externo podem alterar de forma súbita a dinâmica interna de serviços e redes assistenciais, deslocando rapidamente zonas de segurança e de vulnerabilidade.
A pandemia de COVID-19 tornou essa realidade impossível de ignorar. Protocolos existentes mostraram-se insuficientes diante de um evento de rápida disseminação, alta incerteza científica e impacto simultâneo sobre assistência, gestão, economia e comportamento social, mesmo em países com sistemas considerados robustos (WHO, 2022). Instituições tecnicamente bem estruturadas enfrentaram colapsos operacionais; profissionais altamente qualificados vivenciaram insegurança decisória; sistemas com programas de prevenção e controle de infecções formalmente estabelecidos revelaram fragilidades profundas, confirmando que a mera existência de normas e estruturas não garante segurança efetiva.
A resistência microbiana, por sua vez, ilustra de forma silenciosa e cumulativa os limites do pensamento linear. Durante décadas, a resposta predominante ao surgimento de microrganismos resistentes foi a criação de novos antimicrobianos, como se a inovação farmacológica isolada pudesse resolver o problema. Hoje está claro que a resistência é fenômeno complexo, alimentado por padrões de uso em humanos e animais, pressão seletiva no ambiente, modelos de produção de alimentos, fluxos globais e determinantes sociais e econômicos, o que exige abordagens integradas e intersetoriais, em linha com a perspectiva de Saúde Única (LAXMINARAYAN et al., 2013; WHO, 2015).
Eventos climáticos extremos, degradação ambiental e mudanças na produção e circulação de alimentos introduzem ainda novas variáveis no cenário sanitário, ampliando a incerteza e a imprevisibilidade. Surtos, infecções associadas à assistência e crises epidemiológicas deixam de ser eventos excepcionais e passam a compor um pano de fundo permanente de instabilidade, no qual os sistemas de saúde são simultaneamente impactados e coprodutores de risco (WHO, 2022). Nesse contexto, a busca por um controle absoluto revela-se não apenas ilusória, mas potencialmente perigosa, pois pode levar à subestimação de riscos emergentes e ao atraso na adoção de estratégias adaptativas.
O fim das certezas lineares não significa abandonar técnica, ciência ou normatização, mas reconhecer que elas são necessárias, porém insuficientes quando operam isoladamente. Protocolos seguem fundamentais, mas não garantem segurança por si mesmos; evidências científicas são indispensáveis, mas precisam ser interpretadas à luz de contextos específicos, de comportamentos humanos e de dinâmicas institucionais; a especialização permanece valiosa, mas perde eficácia quando descolada de uma visão sistêmica capaz de considerar interdependências e efeitos não lineares (PLSEK; GREENHALGH, 2001; BRAITHWAITE et al., 2018).
Para a prevenção e o controle de infecção, essas mudanças têm implicações profundas. Um modelo apoiado exclusivamente em vigilância retrospectiva, fiscalização de normas e resposta a eventos passados mostra-se limitado em um mundo em transformação acelerada, no qual riscos emergem de interações entre fatores clínicos, organizacionais, ambientais e sociais. A capacidade de antecipar riscos, interpretar sinais precoces, integrar informações de diferentes áreas, compreender interações complexas e atuar de forma coordenada torna-se tão importante quanto o domínio técnico clássico de microbiologia, epidemiologia e farmacologia (WHO, 2022).
Reconhecer que o século XXI rompeu com as certezas lineares que sustentaram a prática em saúde durante décadas é o primeiro passo para reposicionar o controle de infecção. O campo deixa de poder ser visto apenas como executor de protocolos e passa a ser chamado a ocupar lugar central nas decisões estratégicas, contribuindo para a leitura de contexto, a gestão de incertezas e a construção de sistemas mais resilientes (BRAITHWAITE et al., 2018; WHO, 2022). É a partir dessa compreensão que se abre espaço para repensar o papel do profissional, da instituição e dos modelos formativos diante de desafios que não admitem respostas simples nem soluções exclusivamente técnicas.
Capítulo 2 – O mundo BANI e por que a saúde sofre mais
Se o século XXI marcou o fim das certezas lineares, o contexto em que os sistemas de saúde passaram a operar pode ser descrito, de forma particularmente precisa, pelo acrônimo BANI: frágil (brittle), ansioso (anxious), não linear (nonlinear) e incompreensível (incomprehensible) (CASCIO, 2020; KRAAIJENBRINK, 2022). Mais do que um modismo, esse enquadramento oferece uma lente para compreender por que respostas tradicionais – baseadas apenas em planejamento racional, protocolos estáveis e hierarquias rígidas – têm falhado diante de crises sanitárias, ambientais e sociais sucessivas.
A fragilidade diz respeito ao fato de que muitos sistemas foram otimizados ao extremo para eficiência, tornando-se incapazes de absorver choques sem colapsar. No campo da saúde, isso se traduz em serviços que operam permanentemente no limite de sua capacidade, com pouca margem de manobra para enfrentar surtos, desastres, rupturas de cadeias de suprimentos ou crises prolongadas, como evidenciado durante a pandemia de COVID-19 e em avaliações recentes de programas nacionais de prevenção e controle de infecções (WHO, 2022; LEONG et al., 2024). Pequenas disrupções – falta de insumos críticos, rotatividade de pessoal, falhas de infraestrutura – podem desencadear consequências desproporcionais, comprometendo rapidamente a segurança do paciente e do profissional.
A ansiedade é alimentada pela percepção constante de ameaça, pela sobrecarga de demandas e pela sensação de impotência diante de riscos que não podem ser plenamente controlados (CASCIO, 2020; ZEISS, 2025). Profissionais de saúde vivem sob pressão permanente por resultados, sob escrutínio social e institucional, muitas vezes responsabilizados individualmente por falhas que nascem em níveis sistêmicos. Essa ansiedade não é apenas emocional; ela afeta a qualidade da atenção, reduz a capacidade reflexiva, favorece respostas defensivas e reforça a adesão mecânica a normas, em detrimento da compreensão profunda dos processos e dos porquês das práticas.
A não linearidade expressa o fato de que, em sistemas complexos, não há relação proporcional entre causa e efeito: intervenções aparentemente pequenas podem gerar impactos inesperadamente grandes, enquanto grandes esforços podem produzir resultados modestos ou deslocar problemas para outros pontos da rede (PLSEK; GREENHALGH, 2001; BRAITHWAITE et al., 2018). No controle de infecção, isso se manifesta em surtos que emergem sem padrão aparentemente claro, na disseminação rápida de microrganismos resistentes a partir de focos localizados, ou em mudanças súbitas de perfil epidemiológico associadas a alterações ambientais, organizacionais ou comportamentais que não foram adequadamente consideradas.
Por fim, a incompreensibilidade decorre não apenas da complexidade intrínseca dos sistemas, mas também do excesso de dados desconectados, indicadores pouco integrados e informações que não se traduzem em inteligência prática (BRAITHWAITE et al., 2018; WHO, 2022). Serviços de saúde produzem grandes volumes de registros, relatórios e métricas, mas frequentemente carecem de capacidade analítica e de espaços institucionais para transformar esse material em compreensão compartilhada e em decisões alinhadas com a realidade do trabalho cotidiano. O resultado é a sensação de “não entender completamente o que está acontecendo”, ainda que se monitorem múltiplas variáveis em tempo real.
A saúde sofre mais nesse mundo BANI porque concentra, de maneira intensa, todas essas dimensões. Lida diretamente com vidas humanas, com decisões sob forte pressão temporal e emocional, com recursos limitados, com conhecimento científico em rápida transformação e com expectativas sociais crescentes de segurança e transparência. Ao mesmo tempo, carrega legados de modelos organizacionais rígidos, culturas hierárquicas e formações profissionais fortemente ancoradas em lógicas lineares de causa e efeito.
Para a prevenção e o controle de infecção, operar em um mundo BANI implica reconhecer que o problema não se reduz à correta implementação de bundles, à existência de protocolos atualizados ou à realização de treinamentos periódicos. Significa compreender que fragilidade institucional, ansiedade organizacional, não linearidade dos eventos epidemiológicos e dificuldade de leitura sistêmica moldam profundamente a adesão às práticas, a qualidade das decisões e a capacidade de sustentar melhorias ao longo do tempo.
Ignorar essas dimensões equivale a tratar apenas a superfície dos fenômenos, atribuindo falhas a indivíduos ou a “falta de conhecimento”, quando o que está em jogo são sistemas tensionados, culturas que reforçam o improviso e estruturas de poder que desincentivam a transparência e o aprendizado a partir do erro (REASON, 2000; SINGER; VOGUS, 2013). Em contrapartida, reconhecer o mundo BANI como contexto de fundo permite ao controle de infecção reposicionar-se: deixar de atuar apenas como guardião de normas e assumir o papel de tradutor da complexidade, articulando evidências técnicas, comportamento humano e gestão institucional para construir respostas mais adaptativas e resilientes.
Capítulo 3 – Metanoia: conceito, sentido e implicações para a prática em saúde
Diante de um cenário marcado pelo fim das certezas lineares e pela dinâmica frágil, ansiosa, não linear e incompreensível que caracteriza o mundo contemporâneo, torna-se insuficiente falar apenas em atualização técnica, capacitação pontual ou mudança de protocolos. O desafio que se impõe à saúde – e, de modo particular, à prevenção e ao controle de infecções – é mais profundo: diz respeito à forma como profissionais e instituições interpretam a realidade, tomam decisões e atribuem sentido às próprias práticas. É nesse contexto que o conceito de metanoia ganha relevância como chave explicativa e orientadora de mudanças.
Metanoia não se refere a uma alteração superficial de condutas nem a ajustes incrementais em procedimentos; trata-se de uma transformação do modo de pensar, de perceber e de interpretar o mundo. Diferentemente do aprendizado técnico, que amplia repertórios, e de mudanças comportamentais pontuais, que modificam ações específicas, a metanoia opera no nível dos modelos mentais que orientam a identidade profissional e as decisões cotidianas (MEZIROW, 2000; DIRKX, 2018). Ela envolve revisitar premissas que pareciam inquestionáveis, reconhecer limites de esquemas antigos de interpretação e abrir espaço para formas mais complexas de compreender problemas e soluções.
Na saúde, esse tipo de transformação sempre ocorreu, mas muitas vezes de modo lento, difuso e reativo, em resposta a crises ou mudanças externas impostas. Novos conhecimentos científicos e novas tecnologias foram incorporados sem que se questionassem, na mesma intensidade, as estruturas cognitivas e culturais que lhes serviam de suporte (ARGYRIS; SCHÖN, 1978). Em consequência, sobrepuseram-se camadas de técnica a modelos mentais antigos, criando sistemas mais sofisticados, porém não necessariamente mais inteligentes ou capazes de aprender com a própria experiência.
Compreender metanoia como algo distinto de treinamento é fundamental para orientar políticas de formação e desenvolvimento profissional. Treinar significa, em grande medida, ensinar a fazer melhor o que já se faz; aprender, no sentido tradicional, é adquirir novos conhecimentos e habilidades. Metanoia, por sua vez, implica perguntar se aquilo que se faz – e a forma como se pensa sobre isso – ainda faz sentido diante da realidade atual (MEZIROW, 2000). Exige disposição para enfrentar o desconforto cognitivo, reconhecer contradições e abandonar certezas que se tornaram ineficazes, mesmo que sejam familiares e identitariamente importantes.
No campo da prevenção e do controle de infecção, essa distinção é particularmente importante. Durante décadas, a formação predominante esteve centrada na lógica do cumprimento normativo, da vigilância retrospectiva e da resposta a eventos já ocorridos, reforçando uma identidade profissional associada ao controle técnico e à fiscalização de processos. Em um mundo complexo, porém, essa identidade tende a gerar frustração e sensação de irrelevância, pois não oferece ferramentas para lidar com incerteza, com determinantes humanos do risco e com as dimensões organizacionais e políticas dos problemas (BRAITHWAITE et al., 2018; WHO, 2022).
A metanoia, nesse contexto, não significa negar a importância da microbiologia, da epidemiologia ou das normas, mas reposicioná-las em um modelo mais amplo de compreensão da realidade. O foco deixa de ser apenas “o que ocorreu?” e passa a incluir “por que ocorreu?”, “em que contexto ocorreu?” e “quais padrões se repetem e por quê?”, aproximando-se de abordagens de aprendizagem transformadora e de double-loop learning, nas quais não se corrige apenas o erro, mas se revisam também as premissas que o produziram (ARGYRIS; SCHÖN, 1978; ARGyris, 1977; MEZIROW, 2000).
Institucionalmente, a ausência de metanoia se manifesta na persistência de culturas de conformidade, nas quais a prioridade é demonstrar aderência a normas, produzir documentos e responder a exigências externas, sem questionar pressupostos de gestão, estruturas de poder e dinâmicas comportamentais que perpetuam riscos (REASON, 2000; BOYSEN, 2013). Nesses ambientes, erros são tratados como falhas individuais e não como sinais de problemas sistêmicos; prevalecem modelos de aprendizagem de “circuito simples”, que buscam corrigir sintomas sem modificar as regras de fundo que os geram (ARGYRIS; SCHÖN, 1978). O resultado é a repetição de eventos adversos sob novas formas, acompanhada de desgaste profissional e perda de confiança.
A metanoia propõe, portanto, um deslocamento ético e cognitivo. Convida profissionais e instituições a assumirem responsabilidade não apenas pelo cumprimento de normas, mas pela compreensão das consequências de suas decisões em sistemas interdependentes, aceitando que segurança duradoura emerge de culturas que favorecem transparência, reflexão crítica e aprendizagem a partir do erro – características centrais de uma just culture madura (REASON, 2000; BOYSEN, 2013). Esse movimento amplia o horizonte da segurança do paciente, integrando-a à segurança institucional, à sustentabilidade dos sistemas de saúde e à responsabilidade social da prática profissional.
É importante reconhecer que a metanoia não é processo instantâneo nem homogêneo. Ela tende a ocorrer de forma gradual, muitas vezes desencadeada por crises, conflitos, “dilemas desorientadores” ou experiências-limite que colocam em xeque o modo usual de ver o mundo, tal como descrito pela teoria da aprendizagem transformadora de Mezirow (MEZIROW, 2000; FARIAS; SUSMAN, 2021). A pandemia de COVID-19, por exemplo, funcionou como catalisador de metanoia para muitos profissionais e organizações ao expor de forma inequívoca os limites de modelos mentais tradicionais; entretanto, sem espaços estruturados de reflexão e suporte, esse potencial transformador pode se dissipar, dando lugar a tentativas de “retorno ao normal” anterior.
Reconhecer a necessidade de metanoia é admitir que o principal desafio da prevenção e do controle de infecção no século XXI não é apenas técnico, mas cognitivo e cultural. É aceitar que segurança duradoura não emerge da simples soma de procedimentos corretos, mas da capacidade de interpretar contextos complexos, de aprender continuamente e de alinhar decisões técnicas a uma compreensão mais ampla dos sistemas em que se atua (BRAITHWAITE et al., 2018; WHO, 2022). A partir dessa mudança de perspectiva, o controle de infecção pode deixar de ocupar um lugar periférico e defensivo e se aproximar de um papel estratégico na construção de organizações mais seguras, resilientes e capazes de aprender com a própria complexidade.
Capítulo 4 – Do microrganismo ao comportamento: o controle de infecção como campo-chave da metanoia
Durante muito tempo, a prevenção e o controle de infecção foram estruturados sobre um eixo predominantemente microbiológico. Identificar agentes etiológicos, compreender mecanismos de transmissão, diagnosticar infecções e definir terapêuticas adequadas constituiu o núcleo da formação e da prática profissional, sustentando avanços significativos ao longo do século XX. Esse enfoque permanece indispensável, mas, quando adotado como eixo exclusivo de análise e intervenção, torna-se insuficiente para explicar e prevenir a maior parte dos eventos adversos que hoje desafiam sistemas de saúde complexos e tensionados.
As infecções relacionadas à assistência raramente decorrem apenas da presença de microrganismos no ambiente ou no paciente. Elas emergem de cadeias de decisões humanas, de falhas repetidas em processos assistenciais, de culturas organizacionais permissivas e de sistemas que naturalizam desvios em nome da produtividade, da conveniência ou da suposta “praticidade” do trabalho real. Higienização inadequada das mãos, uso indevido ou excessivo de antimicrobianos, quebras rotineiras de barreiras de proteção, comunicação falha entre equipes e priorização de metas de produção em detrimento da segurança são exemplos recorrentes de fatores comportamentais e organizacionais que sustentam o risco infeccioso.
Nesse sentido, deslocar o foco analítico do microrganismo para o comportamento humano e para os sistemas que o moldam não significa negar a microbiologia, mas ampliá-la. O microrganismo deixa de ser visto apenas como inimigo externo a ser combatido e passa a ser compreendido como marcador de fragilidades sistêmicas, indicando problemas em processos, culturas, lideranças e estruturas institucionais. A pergunta central deixa de ser unicamente “qual patógeno está envolvido?” para incluir “quais comportamentos, decisões e contextos permitiram que essa infecção ocorresse e se mantivesse?”.
Quando o campo permanece restrito à lógica do diagnóstico e do tratamento, tende a operar de forma predominantemente reativa. Age após a ocorrência do evento, busca corrigir falhas pontuais e reforça normas já existentes, sem necessariamente questionar as condições que tornam o desvio provável ou até necessário no cotidiano. Em ambientes complexos, essa abordagem produz ganhos limitados e frequentemente temporários: surtos se repetem, taxas de infecção voltam a crescer após intervenções iniciais, e ações educativas pontuais perdem efeito quando não há transformação das dinâmicas organizacionais e da cultura de trabalho.
Ao assumir o comportamento humano como eixo central, o controle de infecção aproxima-se de forma explícita de campos como fatores humanos, psicologia social, segurança do paciente e teoria das organizações. Decisões individuais passam a ser compreendidas não como atos isolados de vontade, mas como respostas a contextos marcados por carga de trabalho, recursos disponíveis, clima organizacional, estilo de liderança, incentivos explícitos e implícitos, mecanismos de reconhecimento e punição e narrativas de “trabalho real” que se consolidam entre pares. Ignorar essas dimensões equivale a esperar resultados diferentes mantendo intactas as condições que produzem os mesmos desfechos.
Essa lógica se estende muito além dos muros hospitalares. O uso indiscriminado de antimicrobianos em humanos e animais, a degradação ambiental, a intensificação da produção agropecuária sem controles sanitários adequados, a urbanização desordenada e o manejo inadequado de resíduos criam condições favoráveis ao surgimento e à disseminação de microrganismos resistentes. Catástrofes ambientais, como enchentes e colapsos de infraestrutura sanitária, ampliam ainda mais esses riscos, evidenciando que infecções e crises epidemiológicas são, em grande medida, consequência acumulada de escolhas humanas, políticas públicas e modelos de desenvolvimento.
É nesse ponto que o controle de infecção se conecta de forma natural ao paradigma da Saúde Única. Ao reconhecer a interdependência entre saúde humana, animal e ambiental, esse paradigma oferece uma base mais adequada para compreender desafios como resistência antimicrobiana, zoonoses emergentes e impacto de mudanças climáticas sobre o perfil de doenças infecciosas. Microrganismos circulam entre diferentes ecossistemas, resistências se desenvolvem em múltiplos contextos e decisões tomadas em setores como agricultura, indústria e urbanismo produzem efeitos diretos sobre os riscos enfrentados nos serviços de saúde.
Assumir o comportamento humano como eixo central implica também redefinir o papel do profissional de controle de infecção. Ele deixa de ser apenas executor de normas ou fiscal de processos e passa a atuar como analista de sistemas, mediador de conflitos, educador e agente de mudança cultural. Essa atuação exige competências que vão além do domínio técnico clássico: capacidade de leitura de contexto, habilidade de comunicação, compreensão de dinâmicas de poder e de cultura organizacional, manejo de resistências e construção de espaços de diálogo e aprendizagem coletiva.
Instituições que reconhecem essa mudança tendem a integrar o controle de infecção às decisões estratégicas de gestão de pessoas, de planejamento assistencial e de governança clínica. Em vez de tratar eventos adversos apenas como falhas individuais, passam a analisá-los como manifestações de padrões sistêmicos, o que favorece intervenções mais sustentáveis e menos centradas na culpabilização. Essa transição aproxima o controle de infecção de agendas como cultura de segurança, just culture, gestão de risco e melhoria contínua, fortalecendo sua relevância institucional.
O movimento “do microrganismo ao comportamento” não representa uma ruptura com a ciência biomédica, mas sua evolução à luz da complexidade contemporânea. Reflete a compreensão de que segurança duradoura não se constrói apenas com protocolos corretos, mas com sistemas capazes de influenciar decisões humanas em contextos desafiadores, oferecendo condições reais para que o comportamento seguro seja possível, provável e valorizado. É essa compreensão que transforma o controle de infecção em campo-chave da metanoia e o posiciona como elemento central para enfrentar os desafios sanitários, organizacionais e éticos do século XXI.
Capítulo 5 – Instituições sem metanoia: por que falham mesmo quando “fazem tudo certo”
Um dos paradoxos mais desconfortáveis dos sistemas de saúde contemporâneos é a ocorrência de falhas graves em instituições que, à primeira vista, parecem cumprir corretamente todas as exigências técnicas e normativas. Protocolos atualizados, comissões formalmente constituídas, indicadores monitorados e auditorias regulares convivem, não raramente, com surtos recorrentes, infecções evitáveis e uma sensação difusa de insegurança entre profissionais e pacientes (WHO, 2022). Esse fenômeno revela um limite central: fazer tudo “certo” no papel não é garantia de segurança quando os modelos mentais que orientam decisões permanecem inalterados.
Instituições sem metanoia tendem a operar sob uma lógica de conformidade. O foco recai sobre demonstrar aderência a normas, produzir documentos, alimentar sistemas de informação e responder a demandas regulatórias, enquanto a compreensão profunda dos processos e das causas sistêmicas dos eventos adversos permanece em segundo plano. A segurança do paciente é reduzida a checklists, e o controle de infecção é percebido como um conjunto de tarefas burocráticas, frequentemente dissociadas da realidade cotidiana do cuidado.
Nesse contexto, instala-se a “ilusão normativa”: a existência de protocolos gera uma sensação de controle, mesmo quando a prática real se distancia sistematicamente do que está prescrito (REASON, 2000). Adaptações informais, atalhos e desvios são incorporados à rotina e normalizados, especialmente em ambientes sobrecarregados, sem que sejam reconhecidos como sinais de fragilidade sistêmica. Indicadores formais podem permanecer aparentemente satisfatórios, enquanto riscos importantes deixam de ser percebidos porque não se enquadram nas métricas usuais.
Outro traço marcante de instituições sem metanoia é a tendência à culpabilização individual. Quando ocorre um evento adverso, a pergunta dominante é “quem errou?”, e não “que condições do sistema favoreceram esse desfecho?”. Essa abordagem reforça comportamentos defensivos, inibe a comunicação aberta sobre falhas e limita o aprendizado organizacional, na contramão do que propõem modelos de just culture e segurança do paciente (REASON, 2000; BOYSEN, 2013).
Nesses ambientes, erros são frequentemente tratados como desvios morais ou falhas de caráter, e não como oportunidades estruturadas de aprendizado. Profissionais passam a ocultar incidentes, evitar o relato de quase falhas e restringir o compartilhamento de dúvidas ou inseguranças, por medo de punições formais ou informais. Com o tempo, consolida-se uma cultura de silêncio, na qual a aparência de controle é preservada às custas da perda de informação crítica para a prevenção de novos eventos.
A ausência de metanoia também se manifesta na maneira como essas instituições lidam com processos educativos. Iniciativas de capacitação são frequentemente reduzidas a treinamentos pontuais, desconectados da realidade do trabalho e da cultura organizacional, focados em transmissão de conteúdo e checagem de presença, sem espaço para reflexão crítica, troca de experiências ou questionamento de pressupostos (MEZIROW, 2000). O conhecimento é oferecido, mas não necessariamente incorporado; diretrizes são apresentadas, mas não discutidas; e a complexidade do cotidiano é pouco considerada na formulação das estratégias de mudança.
No campo específico da prevenção e do controle de infecção, esses padrões produzem consequências especialmente graves. A vigilância tende a ser predominantemente retrospectiva, centrada na notificação e análise de eventos já ocorridos, com pouca ênfase em sinais precoces, fatores de risco contextuais e integração com dados assistenciais, comportamentais e organizacionais (WHO, 2022). A resposta costuma ser tardia, focada em contenção de danos imediatos e reforço pontual de protocolos, sem questionar de forma estruturada as condições que favoreceram o evento.
Em contextos de crise – como pandemias, desastres ambientais ou escassez aguda de recursos –, instituições sem metanoia tendem a recorrer a “mais do mesmo”: mais normas, mais formulários, mais controles e, muitas vezes, mais punições. A tentativa de preservar o funcionamento “normal” em cenários radicalmente alterados leva à intensificação de práticas já conhecidas, em vez de fomentar reflexão e inovação. Isso aprofunda fragilidades, amplia o desgaste profissional e reduz a capacidade de adaptação a situações inéditas.
A falência silenciosa da segurança do paciente ocorre, muitas vezes, nesse intervalo entre a aparência de controle e a realidade da prática. Eventos adversos deixam de ser vistos como exceções e passam a ser naturalizados como “parte do trabalho”, enquanto oportunidades de transformação se perdem em meio à rotina de cumprimento formal de requisitos. Sem metanoia, a instituição pode permanecer tecnicamente correta em termos documentais, mas cognitivamente estagnada, incapaz de aprender com a própria experiência e de antecipar riscos emergentes.
Reconhecer esse padrão é passo fundamental para romper com ele. A metanoia institucional implica deslocar o foco de “como comprovar conformidade” para “como compreender melhor a realidade em que atuamos e os efeitos de nossas decisões”. Exige questionar não apenas procedimentos, mas pressupostos; não apenas condutas individuais, mas estruturas de poder, fluxos de comunicação, prioridades de gestão e mecanismos de reconhecimento e punição (ARGYRIS; SCHÖN, 1978).
Instituições que iniciam esse processo começam a enxergar o controle de infecção não como setor isolado, mas como eixo transversal de gestão, cultura organizacional e segurança do paciente. Ao integrar o olhar da CCIH a decisões sobre dimensionamento de pessoal, desenho de processos, aquisição de tecnologias, planejamento de infraestrutura e gestão de crises, criam condições mais favoráveis à aprendizagem contínua e à construção de sistemas resilientes (WHO, 2022). Deixam de depender exclusivamente de normas para sustentar a segurança e passam a investir em inteligência organizacional, maturidade relacional e coerência entre discurso e prática.
É essa transição – de uma lógica de conformidade para uma lógica de compreensão e aprendizado – que diferencia organizações que apenas sobrevivem de aquelas que conseguem se adaptar e crescer em ambientes BANI. E é nesse movimento que o controle de infecção encontra uma de suas principais oportunidades de redefinir seu papel, passando de “guardião de normas” a protagonista na construção de metanoia institucional.
Capítulo 6 – A carreira do profissional de saúde no mundo BANI: obsolescência, ansiedade e valor estratégico
As transformações descritas até aqui não afetam apenas sistemas e instituições; elas incidem diretamente sobre a trajetória profissional de quem atua na saúde, em especial em áreas altamente expostas à complexidade, como a prevenção e o controle de infecção. No mundo BANI – frágil, ansioso, não linear e incompreensível –, carreiras construídas exclusivamente sobre domínio técnico e cumprimento normativo tornam-se progressivamente vulneráveis, mesmo quando sustentadas por experiência e boa formação inicial.
A obsolescência profissional, nesse contexto, não se limita à defasagem de conhecimentos específicos. Ela se manifesta quando o profissional continua operando com modelos mentais que já não dialogam com a realidade em que está inserido: normas mudam, diretrizes se atualizam, tecnologias se sofisticam, mas a forma de interpretar problemas, tomar decisões e lidar com a incerteza permanece ancorada em pressupostos lineares e previsíveis. O resultado é uma sensação crescente de inadequação diante de demandas que não admitem respostas prontas, reforçando o risco de desengajamento, desgaste e perda de relevância.
Essa condição alimenta um estado de ansiedade crônica. Profissionais de saúde são pressionados a demonstrar controle em ambientes cada vez menos controláveis, a antecipar riscos em sistemas instáveis e a garantir segurança em estruturas frequentemente frágeis, com recursos limitados e expectativas sociais elevadas (WHO, 2022). Quando as ferramentas cognitivas e institucionais disponíveis não acompanham essa complexidade, a ansiedade deixa de ser episódica e passa a fazer parte do cotidiano de trabalho, com impacto sobre bem-estar, tomada de decisão e qualidade do cuidado.
No campo do controle de infecção, essa ansiedade é intensificada pela posição ambígua que o profissional ocupa. Ele é frequentemente responsabilizado por eventos adversos e cobrado por resultados que dependem de múltiplos atores – desde a alta gestão até equipes assistenciais –, mas muitas vezes dispõe de poder limitado para influenciar decisões estratégicas, alocação de recursos ou desenho de processos. Quando seu papel permanece restrito à fiscalização e à atuação reativa, instala-se uma tensão permanente entre responsabilidade formal e capacidade real de intervenção, o que aumenta o risco de desgaste emocional e de sentimento de impotência.
Ao mesmo tempo, o mundo BANI abre uma diferenciação clara entre profissionais que apenas executam funções prescritas e aqueles que desenvolvem valor estratégico. Em ambientes complexos, cresce a demanda por profissionais capazes de interpretar contextos, integrar informações provenientes de áreas distintas, dialogar com diferentes níveis da organização e contribuir para decisões que extrapolam o âmbito técnico imediato (BRAITHWAITE et al., 2018; WHO, 2022). O valor deixa de estar associado apenas ao acúmulo de títulos ou de anos de experiência e passa a residir na capacidade de pensar, conectar e antecipar.
Essa transição redefine o sentido de carreira em saúde. Ascensão profissional deixa de ser apenas resultado de tempo de serviço ou de progressão em estruturas hierárquicas tradicionais e passa a depender da relevância percebida do profissional para os objetivos estratégicos da organização. Aqueles que conseguem traduzir dados em inteligência, normas em decisões contextualizadas e eventos isolados em padrões sistêmicos tendem a se tornar referências, mesmo em contextos de forte pressão e instabilidade. Já os que permanecem presos a modelos estritamente operacionais tendem a experimentar estagnação e insegurança, independentemente de sua competência técnica.
Para o profissional de controle de infecção, essa distinção é particularmente nítida. A complexidade intrínseca do campo o coloca em posição privilegiada para atuar como elo entre assistência, gestão, comportamento humano, vigilância epidemiológica, stewardship de antimicrobianos e segurança do paciente, alinhando-se às recomendações internacionais que enfatizam a centralidade de programas robustos de IPC para a resiliência dos sistemas (WHO, 2022). No entanto, essa possibilidade só se concretiza quando há disposição para repensar a própria identidade profissional e assumir uma postura analítica e estratégica, e não apenas normativa.
Importa destacar que essa mudança não elimina o valor da técnica; ao contrário, exige domínio técnico ainda mais sólido. O que se transforma é o uso que se faz desse domínio: a técnica deixa de ser um fim em si mesmo e passa a ser instrumento a serviço de decisões mais amplas, informadas por leitura de contexto, compreensão sistêmica e sensibilidade às dinâmicas humanas e organizacionais (MEZIROW, 2000; ARGyris; SCHÖN, 1978). Nesse cenário, competências como comunicação, negociação, gestão de conflitos, análise de dados, pensamento crítico e capacidade de facilitar processos de aprendizagem coletiva tornam-se tão importantes quanto o conhecimento microbiológico ou farmacológico.
No mundo BANI, carreiras seguras não são aquelas protegidas da incerteza, mas aquelas capazes de navegar por ela com maturidade cognitiva e emocional. Profissionais que desenvolvem essa capacidade tendem a sofrer menos com a ansiedade, tomar decisões mais consistentes e ampliar seu campo de influência, contribuindo de forma mais efetiva para a segurança de pacientes, colegas e instituições. A diferença não está na ausência de pressão, mas na forma como ela é compreendida, compartilhada e gerida – individual e coletivamente.
Reconhecer esse cenário é essencial para que a discussão sobre formação e desenvolvimento profissional vá além da oferta de cursos e treinamentos pontuais. O que está em jogo é a construção de trajetórias capazes de se sustentar em ambientes instáveis, complexos e em permanente transformação, combinando excelência técnica, metanoia cognitiva e atuação estratégica. Para o controle de infecção, isso significa compreender que a evolução da carreira não se dará apenas pela acumulação de conteúdos e certificações, mas pela capacidade de liderar processos de aprendizagem, de mudança cultural e de construção de sistemas mais inteligentes e resilientes.
Capítulo 7 – Do microrganismo ao comportamento humano: onde realmente nascem as infecções
Durante décadas, a narrativa dominante sobre infecções relacionadas à assistência à saúde foi construída em torno dos microrganismos. Bactérias, vírus, fungos e outros agentes patogênicos ocuparam o centro das atenções, com foco em sua identificação, em seus mecanismos de transmissão, em sua sensibilidade ou resistência a antimicrobianos e em estratégias para eliminá-los do ambiente assistencial. Esse olhar microbiológico foi decisivo para avanços em diagnóstico, terapêutica e prevenção, mas, isoladamente, já não é suficiente para explicar onde, de fato, as infecções “nascem” no cotidiano dos serviços.
A evidência acumulada ao longo dos últimos anos indica que uma parcela importante das infecções poderia ser evitada com medidas simples e bem conhecidas, como higiene adequada das mãos, uso correto de dispositivos invasivos, limpeza e desinfecção de superfícies, aplicação rigorosa de bundles e uso criterioso de antimicrobianos (WHO, 2022). O problema não reside, portanto, apenas na ausência de conhecimento técnico, mas na dificuldade de transformar esse conhecimento em prática consistente, em meio a contextos marcados por sobrecarga, fragmentação de cuidados, comunicação falha e culturas organizacionais que nem sempre priorizam a segurança.
Quando se observa com atenção a trajetória de muitos eventos infecciosos, fica evidente que eles emergem mais do encontro entre microrganismos e comportamentos humanos do que da simples presença de um patógeno no ambiente. São decisões cotidianas – adiar a higiene das mãos, flexibilizar o uso de equipamentos de proteção, prolongar desnecessariamente o uso de cateteres, prescrever antibióticos “por via das dúvidas”, abreviar etapas de limpeza em dias mais corridos – que, somadas, constroem o cenário em que as infecções se tornam prováveis. Em outras palavras, a origem do problema está menos no microrganismo em si e mais na forma como pessoas e sistemas se organizam para lidar com ele.
Isso não significa desvalorizar o conhecimento microbiológico, mas recolocá-lo em relação com determinantes humanos, organizacionais e ambientais. O microrganismo passa a ser entendido como parte de uma rede de interações que envolve práticas profissionais, condições de trabalho, desenho de processos, disponibilidade de recursos, arranjos de equipe, estilos de liderança e políticas institucionais. Assim, prevenir infecções passa a ser, ao mesmo tempo, um desafio técnico, um desafio de comportamento e um desafio de gestão.
Nesse contexto, torna-se fundamental reconhecer a diferença entre “trabalho prescrito” e “trabalho real”. O trabalho prescrito é aquele descrito em protocolos, normas e fluxogramas; o trabalho real é o que acontece na prática, sob pressão de tempo, escassez de pessoal, demandas simultâneas, imprevistos clínicos e conflitos de prioridade. Muitas das decisões que favorecem o surgimento de infecções nascem justamente na lacuna entre esses dois mundos: profissionais ajustam o que fazem para “dar conta” do cotidiano, frequentemente à custa de etapas de segurança que parecem secundárias diante de urgências imediatas.
A compreensão de onde realmente nascem as infecções exige, portanto, aproximação do cotidiano do cuidado. Exige observar rotinas, escutar equipes, mapear trajetórias de pacientes, identificar pontos de pressão e entender como as pessoas tomam decisões em cenários de incerteza e sobrecarga. Exige também reconhecer que comportamentos não são puramente individuais, mas são influenciados por clima de equipe, exemplos de lideranças, políticas de punição ou apoio, reconhecimento ou invisibilidade do trabalho bem feito.
Essa perspectiva reforça a necessidade de integrar o controle de infecção à agenda de cultura de segurança e de just culture. Em instituições nas quais o erro é tratado predominantemente como falha pessoal e não como oportunidade de aprendizado, a tendência é que incidentes relacionados a falhas de processo – por exemplo, lapsos em higiene de mãos, execução incompleta de bundles ou uso inadequado de antimicrobianos – sejam ocultados ou minimizados, dificultando a identificação de padrões. Em contrapartida, ambientes que estimulam o relato aberto, a análise sistêmica e a busca conjunta de soluções tendem a ser mais eficazes em identificar onde, na prática, as infecções estão nascendo e que mudanças são realmente necessárias.
Além do nível micro, em que se situam as interações entre profissionais, pacientes e processos, é preciso considerar o nível meso e o nível macro. No nível meso, decisões sobre dimensionamento de pessoal, investimentos em infraestrutura, escolha de insumos, organização de fluxos e desenho de modelos assistenciais criam condições que podem aumentar ou reduzir o risco de infecções. No nível macro, políticas públicas, financiamento, marcos regulatórios, sistemas de informação e estratégias nacionais de prevenção e controle de infecções e de resistência antimicrobiana moldam o ambiente em que instituições e profissionais atuam (WHO, 2015; WHO, 2022).
Em um mundo interdependente, marcado pelo paradigma da Saúde Única, as infecções também “nascem” em lugares que, à primeira vista, parecem distantes do hospital: na forma como antibióticos são utilizados na comunidade, na pecuária e na agricultura; no manejo de resíduos e efluentes; na ocupação desordenada de territórios; e na maneira como sociedades lidam com mudanças climáticas e degradação ambiental. Essas dimensões ampliam o campo de responsabilidade do controle de infecção, que passa a dialogar com vigilância integrada, stewardship de antimicrobianos e políticas intersetoriais.
Entender que as infecções nascem na interseção entre microrganismo, comportamento humano e contexto sistêmico reforça o lugar do controle de infecção como campo-chave da metanoia. Em vez de se limitar a apontar o “agente causal” do evento, o profissional é chamado a explorar as razões pelas quais aquele agente encontrou condições favoráveis para circular, colonizar e causar dano, identificando padrões de decisão, de comunicação e de organização que precisam ser transformados. Isso exige habilidades analíticas, capacidade de facilitar diálogos interprofissionais e disposição para questionar pressupostos arraigados.
Ao assumir essa perspectiva ampliada, o controle de infecção deixa de ser apenas um conjunto de práticas técnicas e passa a ser um espaço privilegiado de reflexão sobre a forma como se trabalha, se decide e se cuida em saúde. As infecções deixam de ser vistas como “acidentes inevitáveis” ou “fatalidades microbiológicas” e passam a ser compreendidas como sinais de que comportamentos, processos e sistemas precisam ser revistos. É nesse movimento – do microrganismo isolado ao comportamento situado em sistemas complexos – que se encontra uma das maiores oportunidades de transformação para a segurança do paciente e para a própria evolução da prática profissional no século XXI.
Capítulo 8 – Controle de infecção 4.0: dados, epidemiologia e inteligência artificial na linha de frente
A transição do foco exclusivo no microrganismo para o comportamento humano e para os sistemas que o moldam abre espaço para um novo eixo de transformação no controle de infecção: o uso intensivo e inteligente de dados, aliado a ferramentas digitais e à inteligência artificial. Em um mundo BANI, em que eventos se sucedem com rapidez, interdependência e não linearidade, depender apenas de vigilância manual e retrospectiva significa, muitas vezes, chegar sempre atrasado aos problemas. O que se convencionou chamar de “controle de infecção 4.0” nasce exatamente dessa necessidade de antecipar riscos, enxergar padrões ocultos e apoiar decisões em tempo quase real.
A base desse movimento é a compreensão de que a qualidade da resposta em prevenção e controle de infecções está cada vez mais vinculada à qualidade dos dados disponíveis e à capacidade de integrá-los. Sistemas eletrônicos de prontuário, resultados laboratoriais, perfis de resistência, dados de movimentação de pacientes, informações sobre uso de antimicrobianos, registros de adesão à higiene de mãos e de uso de dispositivos invasivos compõem um ecossistema informacional que, quando analisado de forma integrada, pode transformar a maneira como se faz vigilância epidemiológica (WHO, 2022). Em vez de olhar apenas para eventos já consolidados, torna-se possível identificar precocemente mudanças de padrão, aglomeração de casos, cadeias de transmissão prováveis e pontos críticos de processo.
Nesse cenário, a inteligência artificial surge como aliada importante. Modelos de aprendizado de máquina e outras abordagens avançadas permitem correlacionar grandes volumes de dados heterogêneos – laboratoriais, clínicos, administrativos, comportamentais – para prever risco de infecções específicas, sinalizar pacientes ou setores que demandam atenção intensificada e apoiar decisões de alocação de recursos e de foco de auditorias (GASTALDI et al., 2025; WIEMKEN et al., 2024). Aplicações em desenvolvimento incluem: predição de risco de infecção de sítio cirúrgico, identificação precoce de surtos, monitoramento automatizado de higiene de mãos por visão computacional, apoio ao stewardship de antimicrobianos e análise de notas clínicas por processamento de linguagem natural.
Ao mesmo tempo, a digitalização da vigilância – por meio de sistemas eletrônicos assistidos e totalmente automatizados – tem demonstrado potencial para reduzir a carga de trabalho manual da equipe de controle de infecção, liberando tempo para análise qualitativa e ações educativas (SCHOEN et al., 2020). Em vez de revisar exaustivamente prontuários em busca de casos, profissionais podem se concentrar em validar alertas gerados por algoritmos, investigar cadeias de transmissão sugeridas por mapas de contato e conduzir intervenções junto às equipes. Isso se alinha à ideia de que o valor estratégico do profissional não está em tarefas repetitivas, mas na capacidade de interpretar sinais, dialogar com serviços e liderar processos de mudança.
No entanto, a incorporação de dados, ferramentas digitais e inteligência artificial ao controle de infecção não é isenta de desafios. Problemas de qualidade e completude de dados, fragmentação de sistemas de informação, falta de interoperabilidade, limitações de infraestrutura tecnológica, preocupações éticas com privacidade e vigilância, bem como resistência cultural ao uso de algoritmos em apoio à decisão, constituem barreiras importantes à adoção em larga escala (WHO, 2022; ECDC, 2022). Sem enfrentá-las, há risco de produzir soluções tecnicamente sofisticadas, mas pouco úteis no cotidiano, ou de aprofundar desigualdades entre instituições com maior e menor capacidade tecnológica.
Além disso, é crucial reconhecer que dados e algoritmos não substituem o julgamento clínico nem a compreensão contextual do trabalho real. Sistemas digitais indicam onde podem estar os problemas, mas não explicam, por si, por que eles ocorrem nem como transformá-los; essa tarefa continua exigindo presença no campo, escuta das equipes, análise de processos e leitura sensível da cultura organizacional. Em outras palavras, o controle de infecção 4.0 não é um retorno ao tecnicismo, mas uma oportunidade de ampliar a capacidade de ver e compreender a realidade, desde que mantida a centralidade do comportamento humano e da metanoia institucional.
Do ponto de vista da carreira, a emergência desse novo cenário redefine também o perfil de competências desejadas para o profissional de controle de infecção. Além de microbiologia, epidemiologia e farmacologia, ganham destaque habilidades em interpretação de dados, diálogo com equipes de tecnologia da informação, compreensão básica de modelos preditivos, participação em projetos de implantação de sistemas e capacidade de traduzir resultados quantitativos em narrativas significativas para gestores e equipes assistenciais. Profissionais que conseguem ocupar esse espaço de interface entre clínica, gestão e tecnologia tendem a agregar valor estratégico diferenciado às instituições.
Por fim, o controle de infecção 4.0 conecta-se diretamente a agendas globais de fortalecimento de programas de IPC, de enfrentamento da resistência antimicrobiana e de construção de sistemas de saúde mais resilientes. Ferramentas como painéis globais de progresso em IPC, plataformas de dados integrados sobre resistência e vigilância digital de surtos demonstram que o uso inteligente de informação pode apoiar não apenas decisões locais, mas também políticas nacionais e internacionais de prevenção, resposta e preparação para emergências (WHO, 2022; WHO, 2023). Nesse contexto, a metanoia que recolocou o comportamento humano no centro do controle de infecção encontra, nos dados e na inteligência artificial, aliados poderosos para tornar essa mudança de paradigma operacional, sustentável e escalável.
Capítulo 9 – Integração final: controle de infecção como eixo de inteligência e de futuro em saúde
Ao longo dos capítulos anteriores, tornou-se evidente que a prevenção e o controle de infecção, no século XXI, transcendem a condição de campo técnico especializado para assumir o papel de eixo estruturante da inteligência em saúde. A combinação entre fim das certezas lineares, mundo BANI, necessidade de metanoia, centralidade do comportamento humano, perspectiva de Saúde Única e emergência do controle de infecção 4.0 redefine profundamente o que significa “fazer controle de infecção” em instituições complexas.
Nessa nova configuração, programas de prevenção e controle de infecções deixam de ser vistos como um conjunto de normas e rotinas isoladas e passam a ser entendidos como plataformas de leitura da realidade assistencial e organizacional. A vigilância deixa de ser apenas contagem de casos e passa a ser instrumento para entender como se trabalha, como se decide e onde se concentram fragilidades e forças dos sistemas, conectando dados epidemiológicos, práticas cotidianas, cultura de segurança e decisões de gestão (WHO, 2022).
O deslocamento do foco do microrganismo para o comportamento humano e para os sistemas que o moldam, longe de reduzir a importância da microbiologia, amplia seu alcance ao situá-la em redes de interdependência. Microrganismos e perfis de resistência tornam-se indicadores sensíveis de como as instituições lidam com recursos, com pessoas, com tempo, com pressão e com responsabilidade, em um contexto em que a saúde humana está intrinsecamente ligada à saúde animal e ambiental, tal como preconiza o paradigma de Saúde Única.
A metanoia – pessoal e institucional – aparece como condição para que esse reposicionamento se concretize. Profissionais e organizações são chamados a abandonar a ilusão de controle absoluto, a lógica estritamente normativa e a culpabilização individual, substituindo-as por uma abordagem que valorize reflexão crítica, duplo circuito de aprendizagem, just culture e coragem para questionar pressupostos que já não dão conta da realidade (MEZIROW, 2000; ARGyris; SCHÖN, 1978; REASON, 2000).
Nesse cenário, o profissional de controle de infecção deixa de ocupar um lugar periférico, frequentemente associado à fiscalização, e passa a ser agente de inteligência e de articulação. Sua atuação inclui traduzir evidências científicas para contextos concretos, facilitar diálogos entre equipes assistenciais e gestão, interpretar dados quantitativos e qualitativos, apoiar decisões estratégicas, liderar processos de mudança de comportamento e contribuir para a construção de sistemas mais resilientes e adaptativos (BRAITHWAITE et al., 2018; WHO, 2022).
Por outro lado, o controle de infecção 4.0 reforça a ideia de que, em um mundo de alta complexidade, a intuição precisa caminhar junto com a análise. Sistemas eletrônicos de vigilância, uso qualificado de big data, inteligência artificial e ferramentas de epidemiologia digital expandem a capacidade de enxergar padrões, antecipar riscos e direcionar esforços, desde que sejam integrados a uma compreensão contextual da prática e não tratados como substitutos do julgamento humano (WIEMKEN et al., 2024; WHO, 2022).
Por fim, a carreira em controle de infecção, nesse novo horizonte, passa a ser menos sobre “aplicar normas” e mais sobre “criar sentido” em meio à complexidade. Profissionais que desenvolvem competências técnicas sólidas, associadas a pensamento sistêmico, capacidade de lidar com incerteza, habilidade de comunicação e protagonismo em processos de aprendizagem coletiva, tendem a ocupar posições de referência em instituições que desejam sobreviver e evoluir em um mundo BANI.
O futuro do controle de infecção, portanto, não se resume a novos protocolos ou tecnologias, mas à capacidade de alinhar conhecimento microbiológico, compreensão profunda do comportamento humano, uso inteligente de dados e compromisso ético com a segurança em sentido ampliado: do paciente, dos profissionais, das instituições e da própria sociedade. Nesse alinhamento, o campo se consolida não apenas como resposta a crises, mas como um dos principais espaços de construção de lucidez, responsabilidade e esperança na saúde do século XXI.
Capítulo 10 – Formação, educação e desenvolvimento contínuo: construindo a metanoia na prática
Se a metanoia é condição para reposicionar o controle de infecção no centro das decisões em saúde, a forma como se educa e se desenvolve profissionais passa a ser questão estratégica, e não apenas operacional. Não basta atualizar conteúdos ou multiplicar treinamentos pontuais; é necessário repensar concepções de ensino, modalidades de aprendizagem e trajetórias de desenvolvimento ao longo da vida, alinhando-as às demandas de sistemas complexos, ao mundo BANI e ao papel ampliado do controle de infecção.
Organismos internacionais têm destacado a educação em prevenção e controle de infecções como um dos componentes centrais dos programas de IPC bem-sucedidos. Documentos recentes da OMS e da OPAS propõem currículos estruturados tanto para formação inicial (pre-service) quanto para educação em serviço (in-service), com ênfase em competências técnicas, comportamentais e organizacionais necessárias para reduzir IRAS e combater a resistência antimicrobiana (WHO, 2016; WHO, 2025; PAHO, 2024). A mensagem é clara: a educação em IPC deve ser contínua, contextualizada e integrada aos demais componentes do sistema, e não evento isolado.
Entretanto, em muitas instituições, a educação em controle de infecção ainda é conduzida predominantemente em um modelo transmissivo: aulas expositivas, listas de checagem, provas de retenção de conteúdo e treinamentos de “cumprimento obrigatório” voltados a atender exigências regulatórias. Embora esse formato possa ser útil para introduzir conceitos básicos, ele é insuficiente para promover mudanças de comportamento consistentes e, sobretudo, para fomentar metanoia – entendida como transformação da forma de pensar e de interpretar a prática (MEZIROW, 2000).
A literatura sobre aprendizagem transformadora e desenvolvimento profissional em IPC aponta para a necessidade de ambientes educacionais que sejam, ao mesmo tempo, intencionalmente disruptivos e apoiadores. Isso inclui criar espaços em que profissionais possam problematizar experiências, confrontar contradições entre discurso e prática, experimentar novas estratégias e refletir em grupo sobre as implicações éticas, organizacionais e emocionais do cuidado, em vez de apenas receber orientações prontas (MEZIROW, 2000; FARIAS; SUSMAN, 2021). Comunidades de aprendizagem, metodologias ativas e projetos de melhoria baseados no trabalho real surgem, assim, como ferramentas centrais.
O desenvolvimento do profissional de controle de infecção, em particular, tem sido objeto de modelos de competência que combinam domínio técnico, liderança, educação, pesquisa, gestão e capacidade de influenciar sistemas (APIC, 2021; NHS ENGLAND, 2022). Esses modelos descrevem trajetórias que vão do nível inicial ao especialista, destacando a importância de certificações, de experiência prática estruturada, de mentoria e de participação em redes profissionais para consolidar identidades mais estratégicas e menos restritas ao cumprimento normativo. Em outras palavras, não se trata apenas de “treinar para a função”, mas de cultivar uma carreira em IPC.
Do ponto de vista institucional, isso implica investir em programas de educação em IPC que sejam planejados como parte do sistema de governança da qualidade e da segurança, e não como resposta episódica a surtos ou inspeções. Esses programas devem articular conteúdos clínicos e microbiológicos com temas como cultura de segurança, just culture, comunicação, liderança, uso de dados, Saúde Única e tecnologias digitais, espelhando o próprio reposicionamento do controle de infecção no século XXI (WHO, 2016; WHO, 2022; WHO, 2025).
Por fim, a formação em controle de infecção precisa reconhecer a diversidade de públicos: estudantes de graduação, residentes, profissionais recém-ingressos, equipes assistenciais experientes, lideranças clínicas e gestoras, até especialistas em IPC. Cada um desses grupos demanda abordagens pedagógicas específicas, objetivos de aprendizagem diferenciados e estratégias de avaliação adequadas, sempre com o foco comum de transformar conhecimento em prática e prática em reflexão. Assim, a educação deixa de ser apenas instrumento de “transmissão de normas” e passa a ser, ela própria, um campo de metanoia: um espaço em que se aprende não apenas o que fazer, mas a pensar e agir de maneira diferente em um mundo complexo, frágil, ansioso, não linear e, muitas vezes, incompreensível.
Capítulo 11 – Liderança, governança e resiliência: o lugar do controle de infecção na alta gestão
Se o controle de infecção se tornou eixo estratégico da segurança e da sustentabilidade dos sistemas de saúde, sua efetividade passa, inevitavelmente, pela forma como liderança e governança institucional o incorporam às prioridades organizacionais. Não se trata apenas de “apoiar” tecnicamente a CCIH, mas de reconhecer que decisões de alto nível – sobre recursos, prioridades, modelos assistenciais e cultura organizacional – influenciam diretamente o risco de infecções e a capacidade de enfrentá-las (WHO, 2016; WHO, 2022).
Estudos em diferentes contextos indicam que a presença ativa da liderança – não apenas formal, mas engajada – é fator crítico para o sucesso de programas de prevenção e controle de infecções. Entre as práticas mais associadas à redução de IRAS estão: o envolvimento visível da alta direção em metas de prevenção, a comunicação clara de prioridades, a criação de canais de diálogo com equipes de linha de frente, o acompanhamento sistemático de indicadores e o apoio concreto a mudanças de processos e à alocação de recursos (SAINT et al., 2010; WEAVER et al., 2020). Quando a liderança assume publicamente que infecções evitáveis são inaceitáveis e traduz esse compromisso em decisões e investimentos, o controle de infecção deixa de ser tema “da CCIH” e passa a ser responsabilidade compartilhada.
As diretrizes da OMS sobre componentes centrais de programas de IPC reforçam essa visão ao incluir liderança, estrutura de programa e integração com a governança de qualidade e segurança como pilares essenciais, tanto em nível nacional quanto em nível de estabelecimento (WHO, 2016; WHO, 2017). Isso significa que não basta ter profissionais qualificados em IPC; é necessário que existam estruturas formais, linhas de reporte claras, participação em comitês estratégicos, autonomia técnica e canais definidos para que recomendações da CCIH cheguem à mesa onde se tomam as principais decisões.
Nesse contexto, cresce o debate sobre a necessidade de posicionar profissionais de prevenção e controle de infecções em instâncias de alta gestão, seja na diretoria clínica, na diretoria de qualidade e segurança ou mesmo na cúpula executiva. A presença de “voices of IPC” no nível estratégico amplia a capacidade de influenciar políticas internas, de articular diferentes áreas (assistência, suprimentos, engenharia clínica, hotelaria, TI) e de garantir que implicações de risco infeccioso sejam consideradas em decisões de investimento, expansão de serviços, desenho arquitetônico e definição de modelos de cuidado (STORROW; REDDING, 2016; ICHE LEADERSHIP GROUP, 2023).
A discussão sobre liderança e governança em controle de infecção conecta-se diretamente ao conceito de resiliência organizacional. Organizações resilientes são aquelas capazes de antecipar, absorver, adaptar-se e aprender diante de choques – como surtos, pandemias, crises de abastecimento ou mudanças regulatórias –, mantendo níveis aceitáveis de desempenho e segurança (ANDERSEN et al., 2019; HOLLNAGEL, 2017). O controle de infecção, por sua natureza, ocupa posição privilegiada para identificar vulnerabilidades, acompanhar sinais de estresse no sistema e propor ajustes antes que problemas se tornem críticos.
Para que isso se concretize, porém, é preciso que equipes de IPC tenham condições de exercer liderança em múltiplos níveis. A OMS vem enfatizando a necessidade de desenvolver competências específicas de liderança em profissionais de IPC – como comunicação, negociação, gestão de conflitos, condução de mudanças e influência sem autoridade formal – de modo que possam atuar como catalisadores de transformação, e não apenas como especialistas técnicos (WHO, 2023). Estudos recentes mostraram que programas educativos focados na liderança de equipes de IPC podem reduzir conflitos com equipes assistenciais, melhorar adesão a medidas de prevenção e aumentar a eficácia de intervenções multimodais.
Ao mesmo tempo, a liderança institucional precisa compreender que apoiar o controle de infecção não se resume a “dar aval” a protocolos ou campanhas. Implica participar ativamente de análises de eventos adversos, garantir recursos mínimos para funcionamento da CCIH, apoiar intervenções impopulares quando necessário, promover alinhamento entre metas assistenciais e metas de segurança e cultivar uma cultura em que problemas possam ser trazidos à tona sem medo de retaliação (REASON, 2000; WEAVER et al., 2013). Quando essa aliança entre liderança estratégica e liderança técnica em IPC se estabelece, a capacidade de metanoia institucional se amplia.
Em síntese, o capítulo da liderança e da governança mostra que o futuro do controle de infecção dependerá menos de soluções isoladas – um novo antibiótico, um novo bundle, uma nova tecnologia – e mais de como instituições escolhem organizar poder, responsabilidade e aprendizado. Quando a alta gestão reconhece o controle de infecção como eixo de inteligência e resiliência, e quando profissionais de IPC assumem plenamente seu papel de líderes em sistemas complexos, cria-se o terreno para que segurança do paciente, qualidade assistencial e sustentabilidade deixem de ser discursos e passem a ser práticas vividas no cotidiano.
Capítulo 12 – Metanoia em ação: caminhos práticos para transformar o controle de infecção
Depois de percorrer o caminho que vai do microrganismo ao comportamento humano, do pensamento linear à complexidade e do cumprimento normativo à metanoia institucional, resta uma pergunta inevitável: como transformar essas ideias em ação concreta no cotidiano dos serviços de saúde? Ou, em outras palavras, como fazer com que o controle de infecção deixe de ser apenas um discurso avançado e se torne uma prática coerente com os desafios do século XXI?
O primeiro passo é reconhecer que não há soluções únicas nem “receitas universais”. Cada instituição possui sua história, cultura, recursos, prioridades e vulnerabilidades específicas, o que exige abordagens adaptadas e progressivas, e não pacotes importados sem mediação crítica (WHO, 2016; WHO, 2022). Ainda assim, é possível identificar alguns eixos práticos que se repetem em experiências bem-sucedidas de fortalecimento de programas de prevenção e controle de infecções.
Um primeiro eixo diz respeito à construção de uma agenda explícita de metanoia em IPC. Isso implica criar espaços formais e informais de reflexão, em que equipes possam problematizar rotinas, discutir casos, analisar eventos adversos sob perspectiva sistêmica e explorar as tensões entre trabalho prescrito e trabalho real, sem medo de punição (REASON, 2000; MEZIROW, 2000). Reuniões de análise de casos, rounds conjuntos com diferentes setores, grupos de discussão interprofissionais e fóruns de segurança do paciente podem ser redesenhados para incluir perguntas sobre contexto, decisões e padrões organizacionais, e não apenas sobre o “erro imediato”.
Um segundo eixo está na integração efetiva entre controle de infecção, gestão de risco, qualidade assistencial, saúde ocupacional, farmácia clínica, CCIH/CCIRAS, comitês de ética e comissões de segurança do paciente. Em vez de atuar como ilhas, esses grupos podem compartilhar dados, análises e planos de ação, construindo uma visão comum da segurança e evitando duplicação de esforços ou mensagens contraditórias para as equipes (WHO, 2016; WHO, 2022). Ferramentas como planos de ação integrados, indicadores compartilhados e reuniões conjuntas de governança clínica são instrumentos concretos para essa articulação.
Um terceiro eixo envolve o uso inteligente de dados, sem perder de vista o contexto humano. Isso significa avançar na implantação de sistemas eletrônicos de vigilância, no monitoramento contínuo de indicadores de IPC e de resistência antimicrobiana, na exploração de ferramentas de inteligência artificial e de epidemiologia digital, mas sempre articulando esses recursos a processos de feedback compreensíveis e úteis para quem está na linha de frente (WHO, 2022; GASTALDI et al., 2025). Dados devem servir para iluminar, e não para punir; para orientar decisões e apoiar mudanças, e não apenas para compor relatórios.
Um quarto eixo diz respeito ao investimento deliberado em competências de liderança e comunicação em equipes de IPC. Profissionais tecnicamente excelentes, mas sem capacidade de dialogar, negociar, influenciar e articular diferentes atores, terão dificuldade em promover metanoia institucional. Programas de desenvolvimento que incluam temas como liderança em sistemas complexos, gestão de conflitos, técnicas de facilitação de grupos e estratégias de implementação de mudanças aumentam a capacidade da CCIH/CCIRAS de atuar como catalisadora de transformação, e não apenas como área de referência técnica (WHO, 2023; ICHE LEADERSHIP GROUP, 2024).
Por fim, um quinto eixo consiste em alinhar as estratégias de controle de infecção com agendas mais amplas de Saúde Única, sustentabilidade e preparação para emergências. Isso envolve, por exemplo, participar de comitês e redes que discutem resistência antimicrobiana em perspectiva intersetorial, contribuir para planos de contingência para desastres e pandemias, dialogar com setores responsáveis por saneamento, gestão de resíduos, uso de antimicrobianos em animais e vigilância ambiental, e incorporar essas dimensões em planos institucionais de IPC (WHO, 2015; FAO et al., 2025).
Metanoia em ação, portanto, não é um evento único nem uma grande virada súbita, mas um processo acumulativo de pequenas e grandes decisões alinhadas a um novo modo de pensar. Cada vez que uma instituição escolhe analisar um surto como fenômeno sistêmico, e não como culpa individual; cada vez que um dado é usado para aprender, e não apenas para punir; cada vez que o profissional de controle de infecção é convidado à mesa onde se tomam decisões estratégicas, e não apenas para “validar” protocolos, dá-se mais um passo nesse processo.
No limite, o que está em jogo é a capacidade da saúde de se reinventar diante de um mundo que mudou e continuará mudando. O controle de infecção, por sua natureza e posição, reúne elementos únicos para liderar essa reinvenção: transita entre o micro e o macro, conecta clínica e gestão, lida com dados e com pessoas, dialoga com ciência básica e com políticas públicas. Ao assumir conscientemente esse papel, o campo deixa de ser apenas um “custo” ou uma exigência regulatória e se converte em um dos principais investimentos em futuro: futuro dos pacientes, dos profissionais, das instituições e dos sistemas de saúde como um todo.
Capítulo 13 – Conclusão: o que muda quando a mente muda
Chegando ao final deste percurso, torna-se claro que falar de prevenção e controle de infecção no século XXI é muito mais do que discutir técnicas, protocolos ou indicadores. É falar sobre como se entende a saúde em um mundo complexo, frágil, ansioso, não linear e muitas vezes incompreensível; sobre como se pensa risco, segurança, responsabilidade e cuidado em sistemas que já não cabem em modelos lineares de causa e efeito.
Ao longo dos capítulos, foram sendo desmontadas algumas ilusões centrais: a de que bastaria aperfeiçoar normas para garantir segurança; a de que infecções são fenômenos essencialmente microbiológicos; a de que o controle de infecção pode ser um setor periférico, burocrático, desconectado das decisões estratégicas; a de que formação se resume a transmitir conteúdo. Em seu lugar, emergiu uma visão em que comportamento humano, cultura organizacional, liderança, governança, dados, tecnologia e Saúde Única formam um mosaico indissociável.
Nesse mosaico, a metanoia – pessoal e institucional – aparece como fio condutor. Muda-se o foco: do microrganismo isolado para os sistemas que tornam infecções prováveis; do erro individual para as condições que o produzem e o repetem; do cumprimento mecânico de normas para a compreensão crítica de por que e como determinadas práticas fazem sentido em contextos específicos; da vigilância retrospectiva para uma vigilância que busca antecipar, aprender e ajustar continuamente (MEZIROW, 2000; ARGyris; SCHÖN, 1978; REASON, 2000).
O controle de infecção, nesse cenário, deixa de ser apenas defensor de barreiras físicas e químicas contra microrganismos para tornar-se curador de barreiras cognitivas e organizacionais que impedem a mudança. Sua potência não está apenas em “saber o que fazer”, mas em ajudar serviços e pessoas a enxergar o que ainda não é visto, a nomear o que é evitado, a conectar pontos dispersos em narrativas que permitam agir com mais lucidez e responsabilidade.
Ao mesmo tempo, a emergência do controle de infecção 4.0 reforça que a metanoia não se opõe à tecnologia; ao contrário, precisa dela. Dados, sistemas eletrônicos, inteligência artificial e epidemiologia digital ampliam a capacidade de perceber padrões, antecipar riscos e avaliar intervenções, desde que permaneçam ancorados em compreensão humanizada do trabalho real e em um compromisso ético com a segurança e a justiça. Sem metanoia, tecnologias podem apenas reforçar velhas lógicas de controle e culpabilização; com metanoia, tornam-se ferramentas de aprendizado e cuidado.
Por fim, a discussão sobre carreira e liderança mostra que o futuro do controle de infecção será construído por profissionais que aceitem o duplo desafio de aprofundar sua excelência técnica e, ao mesmo tempo, expandir sua maturidade cognitiva, emocional e política. Profissionais dispostos a transitar entre laboratório e leito, entre planilha e conversa difícil, entre diretrizes internacionais e especificidades locais; capazes de atuar como educadores, articuladores, analistas e líderes em sistemas que precisam desesperadamente de pessoas que pensem além do imediato (BRAITHWAITE et al., 2018; WHO, 2022).
O que muda quando a mente muda, portanto, não é só a forma de escrever protocolos ou de contar infecções. Muda quem se considera responsável pelo quê; muda o lugar do controle de infecção dentro das organizações; muda o modo como se olha para o erro, para o risco e para a incerteza; muda o horizonte de possibilidades para pacientes, profissionais e instituições. Em um mundo em que crises sanitárias tendem a se tornar mais frequentes e complexas, essa mudança de perspectiva talvez seja um dos mais importantes investimentos que a saúde pode fazer em seu próprio futuro.
Referências bibliográficas
WHO / OPAS / One Health / IPC
WORLD HEALTH ORGANIZATION. Global report on infection prevention and control. Geneva: WHO, 2022. Disponível em: https://www.who.int/publications/i/item/9789240051164. Acesso em: 20 jan. 2026.[who]
WORLD HEALTH ORGANIZATION. Guidelines on core components of infection prevention and control programmes at the national and acute health care facility level. Geneva: WHO, 2016. Disponível em: https://iris.who.int/bitstream/handle/10665/251730/9789241549929-eng.pdf. Acesso em: 20 jan. 2026.[iris.who]
WORLD HEALTH ORGANIZATION. Core components for infection prevention and control. Geneva: WHO, 2017. Disponível em: https://www.who.int/teams/integrated-health-services/infection-prevention-control/core-components. Acesso em: 20 jan. 2026.[who]
WORLD HEALTH ORGANIZATION. Global action plan on antimicrobial resistance. Geneva: WHO, 2015. Disponível em: https://www.who.int/publications/i/item/9789241509763. Acesso em: 20 jan. 2026.[pmc.ncbi.nlm.nih]
WORLD HEALTH ORGANIZATION. Infection prevention and control pre-service education and training curriculum. Geneva: WHO, 2025. Disponível em: https://www.who.int/publications/i/item/9789240109964. Acesso em: 20 jan. 2026.[who]
PAN AMERICAN HEALTH ORGANIZATION. Infection prevention and control in-service education and training curriculum. Washington, DC: PAHO, 2024. Disponível em: https://www.paho.org/en/documents/infection-prevention-and-control-service-education-and-training-curriculum. Acesso em: 20 jan. 2026.[paho]
FAO et al. One Health in 2025: achievements, turning points and the road ahead. Rome: FAO, 2025. Disponível em: https://www.fao.org/one-health/highlights/one-health-in-2025–achievements–turning-points-and-the-road-ahead/en. Acesso em: 20 jan. 2026.[fao]
ANVISA. Avaliações nacionais sobre gerenciamento de antimicrobianos e prevenção de infecções relacionadas à assistência à saúde. Brasília, 2024. Disponível em: https://www.inaff.org.br/noticias/anvisa-prorroga-avaliacoes-nacionais-sobre-gerenciamento-de-antimicrobianos-e-prevencao-de-infeccoes-relacionadas-a-assistencia-a-saude. Acesso em: 20 jan. 2026.[inaff.org]
Resistência antimicrobiana e Saúde Única
LAXMINARAYAN, R. et al. Antibiotic resistance—the need for global solutions. The Lancet Infectious Diseases, v. 13, n. 12, p. 1057–1098, 2013. DOI: https://doi.org/10.1016/S1473-3099(13)70318-9.[4]
O’NEILL, J. Tackling drug-resistant infections globally: final report and recommendations. London, 2016. Disponível em: https://amr-review.org/Publications.html. Acesso em: 20 jan. 2026.[pmc.ncbi.nlm.nih]
LESLIE, H. et al. Climate change and infectious disease. The Lancet Planetary Health, v. 5, n. 6, p. e379–e380, 2021. DOI: https://doi.org/10.1016/S2542-5196(21)00002-5.[9]
ROCHA, C. F. D.; BERGALLO, H. G. One Health, climate change and emerging infectious diseases. Ciência & Saúde Coletiva, v. 25, supl. 1, p. 67–82, 2020. DOI: https://doi.org/10.1590/1413-81232020257.08172020.[nature]
Complexidade, mundo BANI e sistemas de saúde
PLSEK, P. E.; GREENHALGH, T. The challenge of complexity in health care. BMJ, v. 323, n. 7313, p. 625–628, 2001. DOI: https://doi.org/10.1136/bmj.323.7313.625.[pubmed.ncbi.nlm.nih]
BRAITHWAITE, J. et al. Complexity science in healthcare – aspirations, approaches, applications and accomplishments: a white paper. BMJ Quality & Safety, v. 27, n. 12, p. 990–998, 2018. DOI: https://doi.org/10.1136/bmjqs-2017-007886.[researchers.mq.edu]
CASCIO, J. Facing the age of chaos. Medium, 2020. (texto original sobre BANI, citado indiretamente em análises).[forbes]
KRAAIJENBRINK, J. What BANI really means (and how it corrects your world view). Forbes, 22 jun. 2022. Disponível em: https://www.forbes.com/sites/jeroenkraaijenbrink/2022/06/22/what-bani-really-means-and-how-it-corrects-your-world-view/. Acesso em: 20 jan. 2026.[forbes]
Toward multiplex health: integrating complexity, normativity, and care. Frontiers in Psychology, 2025. DOI: indicado na página do artigo.[frontiersin]
Segurança do paciente, erro humano, cultura e just culture
REASON, J. Human error: models and management. BMJ, v. 320, n. 7237, p. 768–770, 2000. DOI: https://doi.org/10.1136/bmj.320.7237.768.[pmc.ncbi.nlm.nih]
BOYSEN, P. G. Just culture: a foundation for balanced accountability and patient safety. Ochsner Journal, v. 13, n. 3, p. 400–406, 2013. Disponível em: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3776518/. Acesso em: 20 jan. 2026.[pmc.ncbi.nlm.nih]
SINGER, S. J.; VOGUS, T. J. Safety climate research: taking stock and looking forward. BMJ Quality & Safety, v. 22, n. 1, p. 1–4, 2013. DOI: https://doi.org/10.1136/bmjqs-2012-001163.[nature]
WEAVER, S. J. et al. Promoting a culture of safety as a patient safety strategy. Annals of Internal Medicine, v. 158, n. 5, p. 369–374, 2013. DOI: https://doi.org/10.7326/0003-4819-158-5-201303051-00002.[pmc.ncbi.nlm.nih]
Aprendizagem transformadora, metanoia e desenvolvimento profissional
MEZIROW, J. Transformative dimensions of adult learning. San Francisco: Jossey-Bass, 1991.[normfriesen]
MEZIROW, J. An overview on transformative learning. In: ILLERIS, K. (ed.). Contemporary theories of learning. London: Routledge, 2009. Disponível em: https://www.normfriesen.info/files/Mezirows_overview_transformative.pdf. Acesso em: 20 jan. 2026.[normfriesen]
ARGYRIS, C. Double-loop learning in organizations. Harvard Business Review, v. 55, n. 5, p. 115–125, 1977. Disponível em: https://theisrm.org/documents/Argyris%20(1977)%20Double%20Loop%20Learning%20in%20Organizations.pdf. Acesso em: 20 jan. 2026.[theisrm]
ARGYRIS, C.; SCHÖN, D. Organizational learning II: theory, method, and practice. Reading: Addison-Wesley, 1978.[infed]
DIRKX, J. M. Transformative learning theory in the practice of adult education: an overview. Adult Education Quarterly, v. 68, n. 3, p. 247–253, 2018. (Referenciado em análises conceituais).[pmc.ncbi.nlm.nih]
FARIAS, L.; SUSMAN, S. Transformational learning theory (Mezirow). In: ELKJAER, B.; FILIPPOV, K. (eds.). The Routledge Handbook of Adult Learning. London: Routledge, 2021.[taylorfrancis]
Dados, vigilância eletrônica, IA e controle de infecção 4.0
SCHOEN, M. W. et al. Electronically assisted surveillance systems of healthcare-associated infections: a systematic review. Journal of Hospital Infection, v. 104, n. 1, p. 1–14, 2020. DOI: https://doi.org/10.1016/j.jhin.2019.09.010.[pmc.ncbi.nlm.nih]
WIEMKEN, T. L.; KELSEY, M. P.; DESHPANDE, A. Using artificial intelligence in infection prevention and control. Infection Control & Hospital Epidemiology, 2024. DOI indicado na página da revista.[sciencedirect]
Advancing infection prevention and control through artificial intelligence and digital tools. Journal article, 2025. DOI: ver em https://pmc.ncbi.nlm.nih.gov/articles/PMC12722576/.[pmc.ncbi.nlm.nih]
Digital epidemiology: harnessing big data for early detection of infectious diseases. 2024. DOI: ver em https://pmc.ncbi.nlm.nih.gov/articles/PMC11292357/.[pmc.ncbi.nlm.nih]
CCIH MED. Controle de infecção 4.0: epidemiologia, dados e inteligência artificial na linha de frente. 2025. Disponível em: https://www.ccih.med.br/controle-de-infeccao-4-0-epidemiologia-dados-e-inteligencia-artificial-na-linha-de-frente/. Acesso em: 20 jan. 2026.[ccih.med]
Educação, competências e liderança em IPC
WORLD HEALTH ORGANIZATION. Infection prevention and control pre-service education and training curriculum. Geneva: WHO, 2025.[who]
WORLD HEALTH ORGANIZATION. Advanced infection prevention and control training: leadership and programme management. Geneva: WHO, 2023. Disponível em: https://cdn.who.int/media/docs/default-source/integrated-health-services-(ihs)/core-components/advanced-training-leadership.pdf. Acesso em: 20 jan. 2026.[cdn.who]
APIC – ASSOCIATION FOR PROFESSIONALS IN INFECTION CONTROL AND EPIDEMIOLOGY. Infection preventionist (IP) competency model. Arlington, 2021. Disponível em: https://apic.org/professional-practice/infection-preventionist-ip-competency-model/. Acesso em: 20 jan. 2026.[apic]
NATIONAL HEALTH SERVICE ENGLAND. Education framework for the infection prevention and control practitioner. London, 2022. Disponível em: https://www.england.nhs.uk/wp-content/uploads/2022/04/PRN00460-Education-Framework-for-the-Infection-Prevention-and-Control-Prac.pdf. Acesso em: 20 jan. 2026.[england.nhs]
SPICE / UNC. Competency for proficient Infection Preventionists (IPs). Chapel Hill, 2022. Disponível em: https://spice.unc.edu/wp-content/uploads/2022/06/Competency-for-Proficient-IPs-updated-final_2022.pdf. Acesso em: 20 jan. 2026.[spice.unc]
Leadership and programme management in infection prevention and control. WHO Trainer Guide, 2023.[cdn.who]
Liderança, governança e resiliência organizacional
SAINT, S. et al. The importance of leadership in preventing healthcare-associated infections: results of a multisite survey. Infection Control & Hospital Epidemiology, v. 31, n. 9, p. 901–907, 2010. DOI: https://doi.org/10.1086/655459.[pubmed.ncbi.nlm.nih]
Management practices for leaders to promote infection prevention and control. Journal article, 2020. DOI: ver em https://pmc.ncbi.nlm.nih.gov/articles/PMC10302109/.[pmc.ncbi.nlm.nih]
Strengthening the role of hospital leadership in infection prevention and control. Journal article, 2023. DOI: ver em https://pmc.ncbi.nlm.nih.gov/articles/PMC10568750/.[pmc.ncbi.nlm.nih]
Organizational resilience in healthcare: a review and descriptive framework. Journal article, 2023. DOI: ver em https://pmc.ncbi.nlm.nih.gov/articles/PMC10113996/.[pmc.ncbi.nlm.nih]
Hospitals’ resilience: an evidence-based framework for healthcare organisations. Journal of Public Affairs, 2024. DOI: ver em https://onlinelibrary.wiley.com/doi/full/10.1002/pa.70085.[onlinelibrary.wiley]
Executive summary
In the twenty-first century, infection prevention and control has moved beyond a predominantly technical and regulatory function to become a strategic pillar of patient safety, institutional sustainability, and health intelligence. In a context defined by the end of linear certainties and by a BANI world — brittle, anxious, nonlinear, and incomprehensible — approaches centered solely on protocols, retrospective surveillance, and compliance are no longer sufficient. This article argues for a professional and institutional metanoia: a deep transformation of mental models that repositions infection control from an exclusive focus on microorganisms toward an integrated understanding of human behavior, organizational systems, and the interdependence of human, animal, and environmental health. By integrating human factors, safety culture, leadership, governance, and the intelligent use of data and digital technologies, infection control emerges as a key field for risk anticipation, continuous learning, and the construction of more resilient health systems. In this new paradigm, the value of professionals and institutions lies less in formal compliance and more in the ability to interpret complex contexts, integrate evidence, and lead sustainable transformations in the face of twenty-first-century health challenges.
Autor:
Antonio Tadeu Fernandes:
Médico pela FMUSP com residência em Moléstias Infecciosas no HCFMUSP e mestrado em Medicina Preventiva na FMUSP.
Ex-presidente da APECIH e da ABIH.
Autor do livro: “Infecção Hospitalar e suas Interfaces na Área da Saúde” (Prêmio Jabuti como melhor publicação em Ciências Neturais e Saúde).
CEO do Instituto CCIH+
https://www.linkedin.com/in/mba-gest%C3%A3o-ccih-a-tadeu-fernandes-11275529/
https://www.instagram.com/tadeuccih/
#prevenção de infecção #controle de infecção #segurança do paciente #metanoia #mundo bani #comportamento humano #saúde única #resistência microbiana #inteligência artificial na saúde #liderança hospitalar #governança clínica #resiliência organizacional #cultura de segurança #inteligência em saúde #epidemiologia digital #gestão de riscos #sustentabilidade institucional #educação continuada #sistemas complexos #ccih #just culture #aprendizagem transformadora #saúde global #crises sanitárias #controle de infecção 4.0 #estratégia em saúde #antônio tadeu fernandes #instituto ccih #gestão de antimicrobianos #resiliência em sistemas de saúde