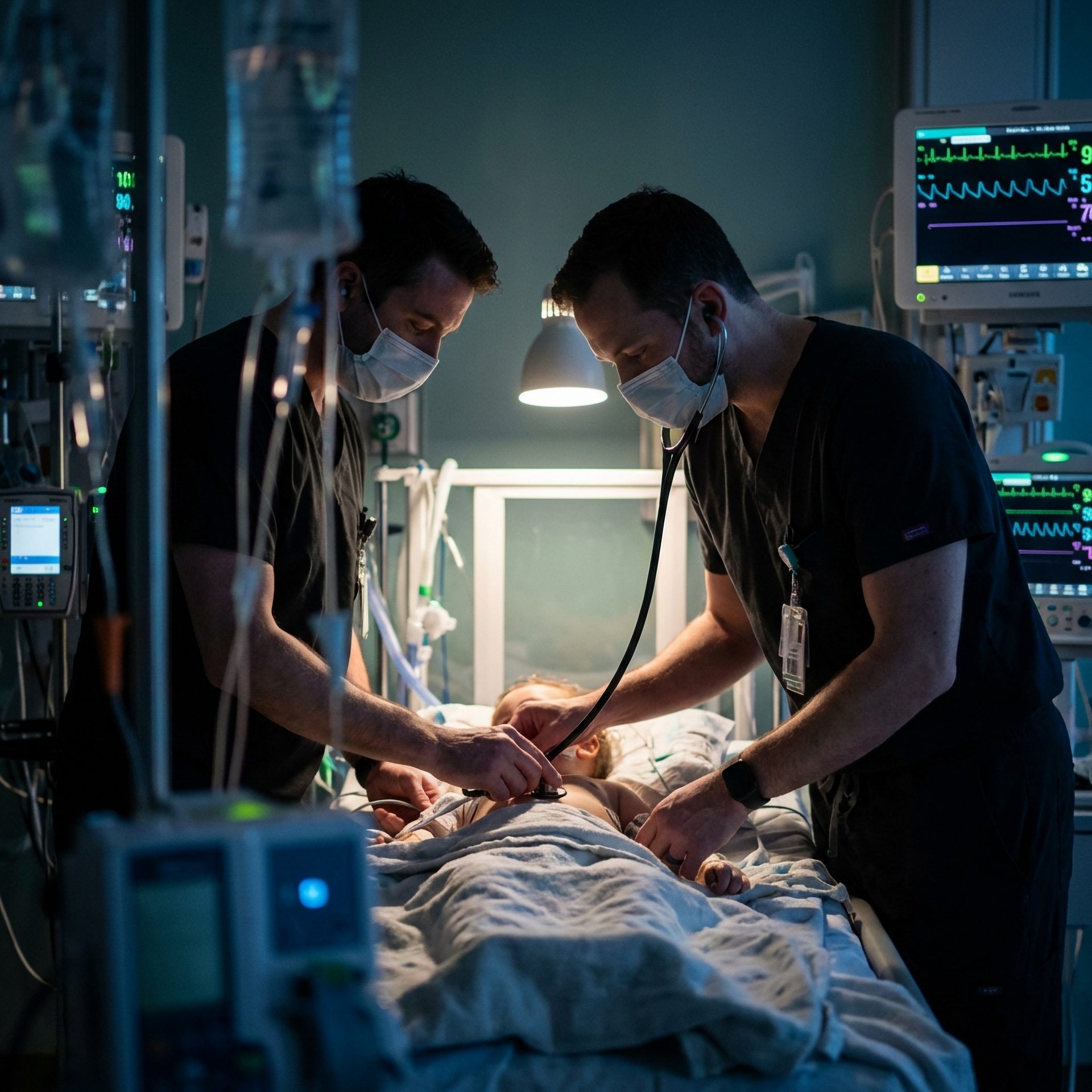
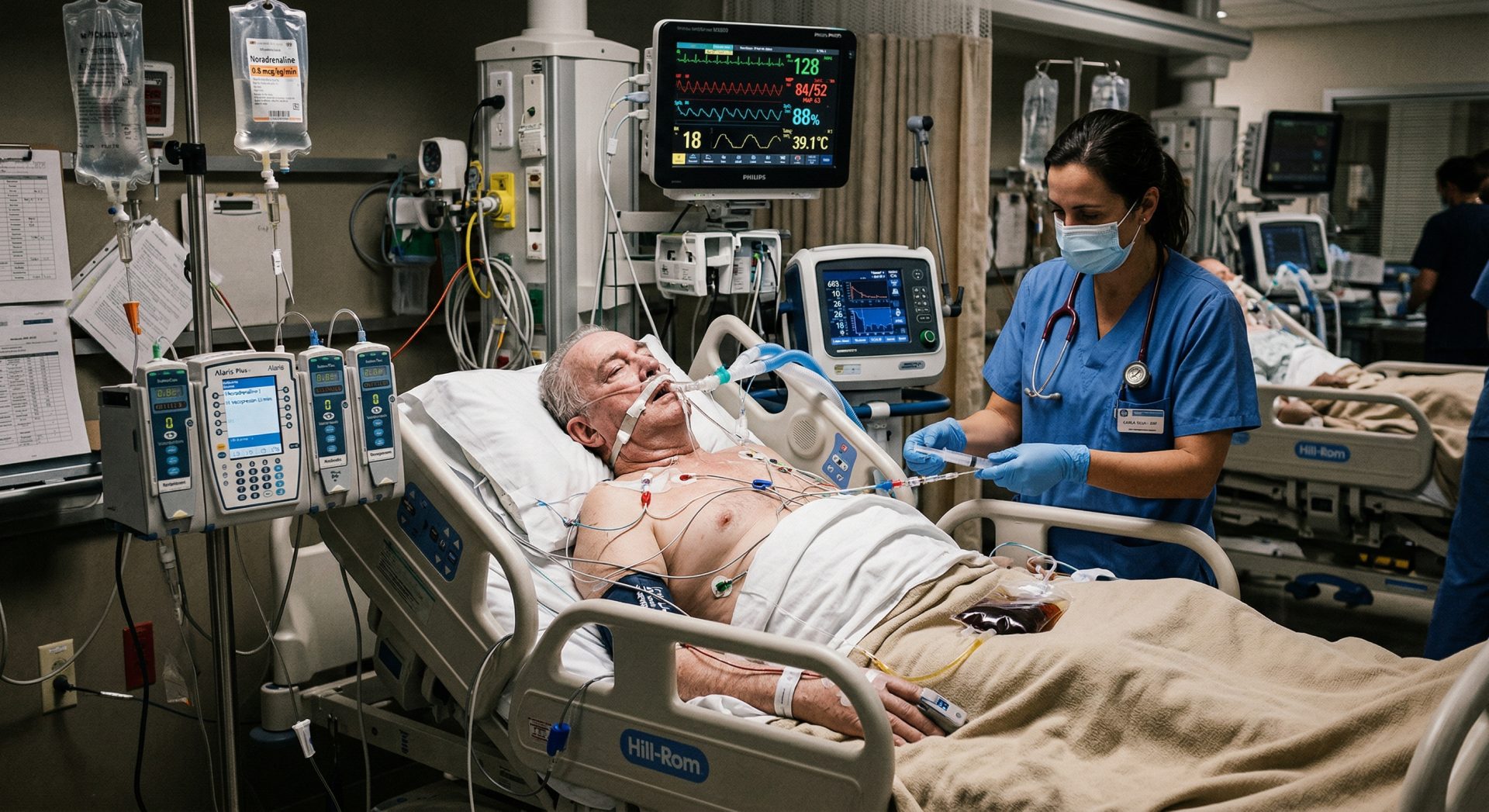
Diagnóstico rápido e decisão certa: a parceria que redefine o controle de infecções.
A crise global da resistência antimicrobiana não será vencida apenas com novos antibióticos. A chave está em transformar diagnósticos rápidos em decisões clínicas seguras — e isso só é possível quando clínicos e o laboratório de microbiologia atuam como parceiros estratégicos.
Este artigo mostra como a Aliança Diagnóstica integra tecnologias como MALDI-TOF e painéis moleculares a programas de Diagnostic Stewardship (DxS) e Antimicrobial Stewardship (ASP). Mais do que inovação tecnológica, trata-se de uma mudança cultural: transformar o laboratório em protagonista na segurança do paciente e no uso racional de antimicrobianos.
FAQ: Diagnóstico Rápido e a Aliança Diagnóstica no Controle de Infecções
Parte I: A Nova Realidade da Microbiologia e o Conceito da Aliança Diagnóstica
Qual é a ideia central da “Aliança Diagnóstica” proposta no artigo?
A Aliança Diagnóstica é a parceria robusta, dinâmica e formalizada entre o clínico e o laboratório de microbiologia. Ela representa a mudança de um modelo reativo, onde o laboratório apenas fornece resultados, para um modelo proativo e colaborativo, onde o laboratório se torna um parceiro estratégico indispensável na tomada de decisão clínica, no uso racional de antimicrobianos e no controle de infecções.
- Referência: Diagnóstico rápido, decisão certa: a parceria que redefine o controle de infecções – ccih.med.br
Por que o artigo afirma que a tecnologia, por si só, é insuficiente para combater a resistência antimicrobiana?
Porque a ponte entre o potencial de um diagnóstico rápido e o desfecho clínico ideal para o paciente não é construída apenas com equipamentos, mas com a colaboração humana. Uma tecnologia avançada é inútil se a amostra for mal coletada (fase pré-analítica) ou se o resultado rápido não for comunicado e interpretado de forma eficaz para gerar uma ação clínica imediata.
- Referência: Diagnóstico rápido, decisão certa: a parceria que redefine o controle de infecções – ccih.med.br
O que é o princípio de “lixo entra, lixo sai” (garbage in, garbage out) na microbiologia?
É o princípio que afirma que a qualidade do resultado de um exame depende diretamente da qualidade da amostra enviada. Uma amostra mal coletada, contaminada, em volume insuficiente ou mal transportada levará a um resultado clinicamente enganoso, mesmo que as tecnologias mais sofisticadas sejam usadas na análise.
O que é Diagnostic Stewardship (DxS) ou Stewardship de Diagnóstico?
É a formalização e estruturação da aplicação criteriosa e inteligente da capacidade diagnóstica. Trata-se de um programa que visa otimizar o uso de exames, garantindo que o teste certo seja solicitado para o paciente certo, no momento certo, e que seus resultados sejam interpretados corretamente para guiar a terapia e maximizar o benefício ao paciente.
- Referência: Terapia antimicrobiana em xeque: estratégias de sobrevivência na era da multirresistência – ccih.med.br
Como o Stewardship de Diagnóstico (DxS) se relaciona com o Stewardship de Antimicrobianos (ASP)?
Eles são parceiros sinérgicos. Um diagnóstico melhor e mais rápido (promovido pelo DxS) é a base para um uso mais eficaz e racional de antimicrobianos (objetivo do ASP). O DxS fornece a informação precisa que permite ao ASP realizar o descalonamento ou a suspensão de antibióticos com segurança.
Quem foi Raymond C. Bartlett e por que sua observação de 1974 ainda é relevante?
Dr. Bartlett foi um patologista clínico visionário que, em 1974, alertou que a capacidade técnica dos laboratórios estava excedendo a habilidade dos médicos de aplicar os testes de forma eficaz. Sua advertência sobre testes “exaustivos, caros e clinicamente irrelevantes” que levam a diagnósticos errôneos é perfeitamente aplicável hoje ao uso indiscriminado de tecnologias como os painéis sindrômicos.
- Referência: Diagnóstico rápido, decisão certa: a parceria que redefine o controle de infecções – ccih.med.br
Qual o risco do uso de painéis sindrômicos sem um contexto clínico rigoroso?
O risco é a detecção de microrganismos que são apenas colonizantes e não a causa da infecção, levando a tratamentos desnecessários e potencialmente danosos. Por exemplo, tratar uma colonização assintomática por Clostridioides difficile ou desviar o foco de uma pneumonia bacteriana por detectar um vírus respiratório incidental.
- Referência: Diagnóstico rápido, decisão certa: a parceria que redefine o controle de infecções – ccih.med.br
Como o artigo define a mudança da “microbiologia reativa” para a “microbiologia proativa”?
A “microbiologia reativa” é o modelo antigo, onde o laboratório apenas processava amostras e liberava laudos dias depois. A “microbiologia proativa” é o novo paradigma, onde o laboratório atua como consultor, comunicando resultados críticos em tempo real, ajudando na interpretação e participando ativamente das decisões clínicas e do controle de infecções.
- Referência: Diagnóstico rápido, decisão certa: a parceria que redefine o controle de infecções – ccih.med.br
Qual o papel da comunicação no sucesso da Aliança Diagnóstica?
É um pilar central. A comunicação eficaz garante que a informação clínica relevante chegue ao laboratório (fase pré-analítica) e que os resultados críticos do laboratório cheguem à equipe clínica de forma rápida e clara, permitindo uma ação terapêutica imediata (fase pós-analítica).
- Referência: Stewardship de antimicrobianos: gerenciando o uso dos antimicrobianos para salvar vidas – ccih.med.br
O que significa a afirmação “a inovação tecnológica não elimina a necessidade do raciocínio clínico; ela a amplifica”?
Significa que, com testes mais sensíveis e rápidos, o volume de informação gerada é muito maior. Isso exige um raciocínio clínico ainda mais apurado para diferenciar colonização de infecção, interpretar achados inesperados e integrar o resultado do exame ao quadro completo do paciente, evitando conclusões precipitadas e tratamentos inadequados.
- Referência: Diagnóstico rápido, decisão certa: a parceria que redefine o controle de infecções – ccih.med.br
Parte II: Para Microbiologistas e a Equipe do Laboratório
Qual o principal papel do laboratório de microbiologia no novo paradigma?
O laboratório deixa de ser um mero prestador de serviços para se tornar um parceiro clínico ativo e indispensável. Seu papel é otimizar as fases analítica e pós-analítica, implementar tecnologias rápidas, comunicar resultados críticos proativamente e atuar como consultor para a equipe clínica na escolha e interpretação dos testes.
- Referência: Diagnóstico rápido, decisão certa: a parceria que redefine o controle de infecções – ccih.med.br
Como a tecnologia MALDI-TOF (espectrometria de massa) transforma a rotina do laboratório?
O MALDI-TOF revoluciona a identificação de microrganismos (bactérias e leveduras), reduzindo o tempo de identificação de 24-48 horas para minutos. Essa velocidade permite liberar resultados muito mais cedo, possibilitando o início da terapia antimicrobiana direcionada com um a dois dias de antecedência.
- Referência: Terapia antimicrobiana sem segredos: os princípios que salvam vidas e evitam resistência – ccih.med.br
Qual a importância de o laboratório ser notificado sobre a suspeita de patógenos de alto risco (ex: Brucella)?
É uma questão de biossegurança. Patógenos como Brucella spp. ou Francisella tularensis representam um alto risco de infecção para a equipe do laboratório. A notificação prévia permite que os microbiologistas manipulem a amostra em uma cabine de segurança biológica, utilizando equipamentos de proteção individual adequados para prevenir a exposição e a infecção laboratorial.
- Referência: Mandell, Douglas, and Bennett’s Principles and Practice of Infectious Diseases – Elsevier Shop (livro citado no artigo)
Quais são as responsabilidades do laboratório na fase pós-analítica?
As responsabilidades incluem garantir a precisão dos resultados, comunicar laudos críticos (ex: hemocultura positiva, identificação de patógeno multirresistente) de forma imediata e eficaz, e estar disponível para discutir a interpretação dos resultados com a equipe clínica, auxiliando na correlação com o quadro do paciente.
- Referência: Diagnóstico rápido, decisão certa: a parceria que redefine o controle de infecções – ccih.med.br
Como o laboratório pode ajudar a melhorar a qualidade da fase pré-analítica?
O laboratório pode e deve liderar iniciativas de educação continuada para as equipes clínicas e de enfermagem sobre a importância e as técnicas corretas de coleta de amostras. Além disso, pode implementar critérios claros de rejeição para amostras inadequadas, fornecendo feedback construtivo para evitar a repetição de erros.
O que são painéis moleculares sindrômicos e qual sua principal vantagem?
São testes, geralmente baseados em PCR multiplex, que detectam simultaneamente múltiplos patógenos (vírus, bactérias, fungos) e, por vezes, genes de resistência, a partir de uma única amostra. Sua principal vantagem é a velocidade e a abrangência, fornecendo um diagnóstico diferencial rápido para síndromes como sepse, meningite ou infecções respiratórias.
- Referência: Diagnóstico rápido, decisão certa: a parceria que redefine o controle de infecções – ccih.med.br
O laboratório deve ter um sistema formal para comunicação de valores críticos?
Sim, é fundamental. O laboratório deve ter um protocolo claro definindo quais resultados são considerados críticos (ex: positividade de líquor ou hemocultura), quem deve ser notificado (médico, enfermeiro, CCIH), por qual meio (ex: contato telefônico) e como essa comunicação deve ser registrada (data, hora, nome do receptor da informação).
Como a informação clínica fornecida pelo médico ajuda o trabalho do microbiologista?
Informações como suspeita clínica, local da infecção, uso prévio de antimicrobianos e comorbidades são vitais. Elas guiam o microbiologista na escolha dos meios de cultura mais adequados, na priorização do processamento e, principalmente, na interpretação dos resultados, ajudando a diferenciar um achado significativo de um contaminante.
- Referência: Mandell, Douglas, and Bennett’s Principles and Practice of Infectious Diseases, 10th Edition – Elsevier Health (livro citado no artigo)
O que o microbiologista deve fazer ao identificar um perfil de resistência incomum ou um surto potencial?
Deve alertar imediatamente a Comissão de Controle de Infecção Hospitalar (CCIH). Essa comunicação rápida é o gatilho para a investigação epidemiológica, a busca ativa de outros casos e a implementação de medidas de bloqueio para conter a disseminação do patógeno.
- Referência: Diagnóstico rápido, decisão certa: a parceria que redefine o controle de infecções – ccih.med.br
Como o laboratório pode contribuir para as métricas do programa de stewardship (ASP)?
O laboratório fornece dados essenciais para o ASP, como os perfis de sensibilidade locais (microbiologia epidemiológica), a frequência de patógenos resistentes e o tempo entre a coleta e a liberação do resultado do antibiograma. Esses dados permitem ao ASP criar protocolos empíricos mais assertivos e medir o impacto das intervenções.
- Referência: Stewardship de antimicrobianos: gerenciando o uso dos antimicrobianos para salvar vidas – ccih.med.br
Parte III: Para Médicos, Farmacêuticos e Enfermeiros
Quais são as principais responsabilidades do clínico na Aliança Diagnóstica?
As principais responsabilidades do clínico concentram-se na fase pré-analítica: selecionar o teste correto para a suspeita clínica, realizar a coleta adequada da amostra (técnica, volume, local e momento corretos), fornecer o máximo de contexto clínico na solicitação do exame e agir prontamente com base nos resultados recebidos.
- Referência: Diagnóstico rápido, decisão certa: a parceria que redefine o controle de infecções – ccih.med.br
Por que é crucial coletar culturas (especialmente hemoculturas) antes de iniciar os antimicrobianos?
A administração de antimicrobianos antes da coleta pode “esterilizar” a amostra, ou seja, inibir ou matar os microrganismos presentes, levando a um resultado falso-negativo. Isso impede a identificação do agente causador da infecção e a realização do teste de sensibilidade, dificultando a terapia direcionada.
- Referência: Mandell, Douglas, and Bennett’s Principles and Practice of Infectious Diseases – Elsevier Shop (livro citado no artigo)
Como um médico deve agir ao receber um resultado de identificação rápida de um patógeno em uma hemocultura?
Deve reavaliar imediatamente a terapia antimicrobiana empírica. Se o tratamento em uso não for adequado para o patógeno identificado, ele deve ser escalonado. Se o tratamento for de espectro muito amplo e o patógeno for sensível a drogas mais específicas, ele deve ser descalonado. A ação deve ser imediata.
- Referência: Stewardship de antimicrobianos: gerenciando o uso dos antimicrobianos para salvar vidas – ccih.med.br
Qual o papel do farmacêutico clínico na interpretação de um resultado rápido?
O farmacêutico clínico é um ator chave no time de stewardship. Ao receber o resultado, ele pode analisar a prescrição, verificar a adequação da dose, via e frequência do antimicrobiano, e sugerir ativamente ao médico o descalonamento ou a otimização da terapia com base no perfil do paciente e no resultado microbiológico.
Como a equipe de enfermagem garante a qualidade da fase pré-analítica?
A enfermagem está na linha de frente da coleta de muitas amostras, como hemoculturas e swabs. A execução rigorosa da técnica asséptica, a coleta do volume correto de sangue e a correta identificação da amostra são ações de enfermagem que impactam diretamente a qualidade e a confiabilidade do diagnóstico.
O que um clínico deve fazer antes de solicitar um painel molecular sindrômico?
Deve se fazer duas perguntas-chave: “Este teste é indicado para este paciente com esta síndrome clínica?” e “O que eu farei com cada um dos possíveis resultados deste painel?”. Isso evita a realização de testes desnecessários e a confusão gerada por resultados clinicamente irrelevantes.
- Referência: Diagnóstico rápido, decisão certa: a parceria que redefine o controle de infecções – ccih.med.br
Ao receber a comunicação de um resultado crítico, o que o profissional de saúde deve fazer?
Deve anotar o resultado, o nome do profissional do laboratório que o contatou e o horário. Em seguida, deve agir imediatamente conforme o resultado, seja ajustando a terapia, seja implementando medidas de isolamento, e registrar todas as ações e decisões no prontuário do paciente.
- Referência: Diagnóstico rápido, decisão certa: a parceria que redefine o controle de infecções – ccih.med.br
Como a identificação rápida de um patógeno multirresistente afeta o trabalho da enfermagem?
A enfermagem deve, sob orientação da CCIH, implementar imediatamente as medidas de precaução de contato ou outras precauções específicas. Isso inclui o uso correto de EPIs (luvas, avental), a higiene rigorosa das mãos e o manejo adequado do ambiente e dos equipamentos para prevenir a transmissão do patógeno para outros pacientes.
É apropriado ligar para o laboratório de microbiologia para discutir um caso?
Sim, é altamente recomendado. O artigo enfatiza a necessidade de uma comunicação bidirecional. Discutir o caso com o microbiologista pode fornecer insights valiosos sobre a relevância de um achado, a necessidade de testes adicionais ou a melhor forma de interpretar um resultado complexo.
- Referência: Diagnóstico rápido, decisão certa: a parceria que redefine o controle de infecções – ccih.med.br
Um resultado rápido pode ajudar a decidir pela alta de um paciente?
Sim. Por exemplo, em uma suspeita de sepse, um painel molecular de hemocultura que resulta negativo rapidamente, associado à melhora clínica do paciente, pode dar à equipe a segurança necessária para suspender antibióticos e programar a alta hospitalar, liberando o leito e reduzindo os riscos de infecção hospitalar.
- Referência: Stewardship de antimicrobianos: gerenciando o uso dos antimicrobianos para salvar vidas – ccih.med.br
Parte IV: Para Gestores Hospitalares e Membros da CCIH
Por que um gestor hospitalar deve investir na Aliança Diagnóstica?
Porque o investimento na integração entre laboratório e equipe clínica, apoiado por tecnologias rápidas, gera um retorno comprovado em múltiplos níveis: reduz a mortalidade e o tempo de internação, otimiza o uso de antimicrobianos (reduzindo custos), melhora a segurança do paciente e fortalece a reputação da instituição.
- Referência: Diagnóstico rápido, decisão certa: a parceria que redefine o controle de infecções – ccih.med.br
Qual o papel da CCIH na promoção da parceria clínico-laboratorial?
A CCIH é a catalisadora natural dessa parceria. Ela deve facilitar a comunicação entre os setores, promover reuniões clínicas conjuntas, desenvolver protocolos assistenciais que incorporem o uso racional de diagnósticos rápidos e monitorar o impacto dessa integração nos indicadores de infecção e consumo de antimicrobianos.
O investimento em diagnóstico rápido é apenas um custo ou pode gerar economia?
Embora exija um investimento inicial, o diagnóstico rápido gera economia significativa a médio e longo prazo. A redução de diárias de internação (especialmente em UTI), a diminuição do uso de antibióticos de amplo espectro (mais caros) e a prevenção de surtos (que têm custos altíssimos) geralmente superam o custo da tecnologia.
- Referência: Diagnóstico rápido, decisão certa: a parceria que redefine o controle de infecções – ccih.med.br
Quais são os principais desafios para implementar a Aliança Diagnóstica?
Os desafios incluem superar a cultura de trabalho em “silos” (setores isolados), integrar os sistemas de informação do laboratório com o prontuário eletrônico do paciente, criar fluxos de comunicação eficientes que funcionem 24/7, e investir em educação e treinamento contínuo para todas as equipes envolvidas.
- Referência: Diagnóstico rápido, decisão certa: a parceria que redefine o controle de infecções – ccih.med.br
Como a CCIH utiliza os dados gerados pelo diagnóstico rápido para a vigilância epidemiológica?
A identificação rápida de patógenos multirresistentes ou de aglomerados de infecções pelo mesmo agente permite que a CCIH atue de forma quase instantânea. Ela pode iniciar a investigação de surto, rastrear contatos e implementar medidas de contenção muito antes do que seria possível com métodos tradicionais, prevenindo a disseminação.
- Referência: Canal no YouTube – CCIH de A a Z, além do óbvio (pesquisar vídeos sobre investigação de surtos)
Como justificar o investimento em um sistema de TI para integrar o laboratório ao prontuário eletrônico?
A justificativa deve focar na segurança do paciente e na eficiência. A integração elimina falhas de comunicação, garante que o resultado certo chegue ao prontuário do paciente certo em tempo real, cria alertas automáticos para resultados críticos e permite a coleta de dados para monitoramento de indicadores de qualidade e desempenho.
- Referência: Diretriz Gerenciamento Antimicrobianos – ANVISA 2023 (Componente Monitoramento) – Portal Gov.br
O que a ANVISA preconiza sobre a estrutura mínima para um Programa de Gerenciamento de Antimicrobianos (PGA)?
A ANVISA preconiza que um PGA deve ter, no mínimo, apoio da alta gestão, um time multidisciplinar (composto por médico, farmacêutico e preferencialmente infectologista e microbiologista), ações para melhorar o uso de antimicrobianos (como protocolos e auditorias), monitoramento de dados e ações de educação. O laboratório de microbiologia é um componente essencial dessa estrutura.
Como a CCIH e os gestores podem medir o sucesso da implementação de diagnósticos rápidos?
O sucesso pode ser medido por um conjunto de indicadores de processo e de resultado, como: redução no tempo para identificação do patógeno, redução no tempo para início da terapia adequada, queda no consumo de antimicrobianos de amplo espectro (medido em DDD), diminuição do tempo de internação e redução nas taxas de mortalidade por infecções graves como a sepse.
- Referência: Diagnóstico rápido, decisão certa: a parceria que redefine o controle de infecções – ccih.med.br
É necessário ter um infectologista no time para que a Aliança Diagnóstica funcione?
Embora a presença de um infectologista seja altamente recomendada e fortaleça enormemente o programa, a aliança pode começar com a colaboração entre os microbiologistas, farmacêuticos clínicos e médicos prescritores. O importante é criar os canais de comunicação e o compromisso de trabalhar em conjunto, com a CCIH facilitando esse processo.
Qual é a conclusão final do artigo sobre o futuro do controle de infecções?
A conclusão é que o futuro do controle de infecções e o combate à resistência antimicrobiana dependem da aplicação inteligente e integrada das ferramentas diagnósticas. Isso requer um compromisso institucional para quebrar barreiras e transformar a relação clínico-laboratorial em uma verdadeira Aliança Diagnóstica, centrada na segurança do paciente e na preservação dos antimicrobianos para as gerações futuras.
- Referência: Diagnóstico rápido, decisão certa: a parceria que redefine o controle de infecções – ccih.med.br
A Nova Fronteira da Microbiologia Clínica e o Imperativo da Colaboração
A medicina contemporânea encontra-se em um ponto de inflexão. De um lado, testemunhamos uma revolução diagnóstica, impulsionada por tecnologias que permitem a identificação de patógenos com uma velocidade e precisão sem precedentes (Ref. 1, 2). Do outro, enfrentamos a crise global da resistência antimicrobiana (RAM), uma pandemia silenciosa que ameaça reverter décadas de progresso médico (Ref. 3). Neste cenário de alto risco e alta tecnologia, torna-se evidente que o avanço tecnológico, por si só, é insuficiente. A ponte entre o potencial de um diagnóstico rápido e o desfecho clínico ideal para o paciente não é construída apenas com equipamentos sofisticados, mas com uma aliança robusta, dinâmica e formalizada: a parceria entre o clínico e o laboratório de microbiologia clínica.
Este artigo explora a profundidade e a criticidade dessa colaboração, argumentando que ela representa a pedra angular da gestão moderna de doenças infecciosas e do controle de infecção hospitalar. A otimização desta aliança é fundamental para garantir a qualidade assistencial, orientar intervenções terapêuticas adequadas, controlar custos e, crucialmente, promover o uso racional de antimicrobianos (Ref. 4). Analisaremos como a integração de inovações, como a espectrometria de massa (MALDI-TOF) e os painéis sindrômicos, com programas de stewardship de antimicrobianos e de diagnóstico, transforma o laboratório de um mero prestador de serviços em um parceiro ativo e indispensável na tomada de decisão clínica. A era da microbiologia reativa terminou; a era da microbiologia proativa, colaborativa e integrada começou.
O Eixo Central da Colaboração: Uma Análise da Relação Clínico-Laboratório
O principal achado que emerge de uma análise aprofundada da prática diagnóstica moderna é que o cuidado ideal de pacientes com doenças infecciosas depende fundamentalmente de uma colaboração fluida e bidirecional entre os médicos assistentes e o laboratório de microbiologia clínica (Ref. 1). Esta não é apenas uma recomendação de boas práticas, mas sim o alicerce sobre o qual se constrói a segurança do paciente, a eficácia terapêutica e a sustentabilidade do nosso arsenal antimicrobiano.
Esta relação pode ser compreendida como um sistema sinérgico, onde a qualidade da fase pré-analítica (responsabilidade primária do clínico) determina diretamente o valor e a utilidade das fases analítica e pós-analítica (domínio do laboratório e da ação clínica subsequente) (Ref. 5, 6). Uma falha em qualquer ponto deste ciclo compromete todo o processo, tornando inúteis até as tecnologias mais avançadas. O princípio de “lixo entra, lixo sai” (garbage in, garbage out) é particularmente verdadeiro na microbiologia: uma amostra mal coletada, contaminada ou inadequadamente transportada levará, inevitavelmente, a um resultado clinicamente enganoso, independentemente da sofisticação do teste realizado (Ref. 1, 7). Da mesma forma, um resultado laboratorial preciso e rápido que não é comunicado de forma eficaz, ou sobre o qual não se age prontamente, torna-se clinicamente inerte.
Essa interdependência intrínseca revela uma verdade fundamental: os investimentos em tecnologia laboratorial devem ser acompanhados por investimentos equivalentes em educação clínica, otimização de fluxos de trabalho e infraestrutura de comunicação. Uma instituição de saúde não pode simplesmente adquirir um espectrômetro de massa ou um sistema de painel molecular e esperar uma melhoria automática nos desfechos. É imperativo fortalecer simultaneamente os sistemas humanos que alimentam, interpretam e atuam com base nos resultados gerados por essas tecnologias.
Fundações do Conhecimento: A Evolução da Interdependência Diagnóstica
A discussão atual sobre a necessidade de uma colaboração mais estreita não é inteiramente nova. Ela ecoa as advertências de figuras visionárias da patologia clínica, como o Dr. Raymond C. Bartlett, que, já em 1974, observou que “nossas capacidades técnicas estão excedendo nossa habilidade de aplicá-las de forma eficaz e econômica aos problemas humanos” (Ref. 2). Ele alertou contra a pressão para realizar testes “exaustivos, caros e clinicamente irrelevantes” que, quando mal orientados, “induzem os médicos a diagnósticos errôneos e terapias inadequadas” (Ref. 2).
Essa perspectiva histórica é crucial, pois demonstra que os desafios enfrentados hoje com os complexos diagnósticos moleculares são, em essência, os mesmos enfrentados no passado com os métodos convencionais. A advertência de Bartlett é perfeitamente aplicável ao risco atual dos painéis sindrômicos multiplex quando utilizados sem um contexto clínico rigoroso. Por exemplo, a detecção de um vírus respiratório em um paciente com clara pneumonia bacteriana pode desviar o tratamento, assim como a identificação incidental de Clostridioides difficile em um painel gastrointestinal pode levar ao tratamento inadequado de uma colonização assintomática (Ref. 9, 10).
Este paralelo histórico valida a perenidade dos princípios de correlação clínico-laboratorial e de stewardship. A necessidade de questionar “Este teste é indicado para este paciente?” e “O que farei com o resultado?” é uma constante, independentemente da tecnologia empregada. A inovação tecnológica não elimina a necessidade do raciocínio clínico fundamental; pelo contrário, ela a amplifica. O conceito moderno de Diagnostic Stewardship (DxS), ou stewardship de diagnóstico, não é, portanto, uma ideia radicalmente nova, mas a formalização e a estruturação de uma necessidade há muito reconhecida: a aplicação criteriosa e inteligente da capacidade diagnóstica para maximizar o benefício ao paciente (Ref. 8).
Estruturando a Parceria: Responsabilidades Mútuas e Comunicação Efetiva
Para que a aliança diagnóstica funcione, é essencial delinear e respeitar um conjunto de responsabilidades mútuas que abrangem todo o ciclo do teste diagnóstico, desde a solicitação até a ação clínica.
Responsabilidades do Clínico: A Maestria da Fase Pré-Analítica
O papel do clínico é fundamental e vai muito além da simples solicitação de um exame. Ele é o guardião da fase pré-analítica, e sua diligência nesta etapa é o fator mais crítico para o sucesso diagnóstico (Ref. 1). Suas responsabilidades incluem:
- Seleção Criteriosa do Teste: Compreender o menu de testes do laboratório, suas indicações, limitações, sensibilidade e especificidade para selecionar o exame mais apropriado para a suspeita clínica.
- Coleta Adequada da Amostra: Garantir que a amostra seja representativa do sítio da infecção, coletada com técnica asséptica para evitar contaminação, em volume suficiente e no momento clínico ideal (preferencialmente antes do início de antimicrobianos). A coleta de amostras do trato respiratório inferior, por exemplo, é crucial quando há suspeita de pneumonia e as amostras contaminada com microrganismos do trato superior não tem validade habitualmente (Ref. 11).
- Fornecimento de Contexto Clínico: A informação clínica relevante (ex: suspeita de endocardite, viagem recente, condição de imunossupressão) é vital para que o laboratório otimize o processamento, selecione meios de cultura adequados e interprete os achados corretamente.
- Alerta sobre Riscos Biológicos: Notificar proativamente o laboratório sobre a suspeita de patógenos de alto risco (ex: Brucella spp., Francisella tularensis, fungos dimórficos) para garantir o manuseio seguro das amostras em cabines de segurança biológica (Ref. 1).
Responsabilidades do Laboratório: Excelência Analítica e Comunicação Pós-Analítica
O laboratório, por sua vez, tem a responsabilidade de garantir a precisão e a relevância clínica de seus resultados, atuando como um consultor ativo para a equipe assistencial (Ref. 1). Suas funções englobam:
- Curadoria do Menu de Testes: Manter um menu de testes atualizado, clinicamente relevante e custo-efetivo. Esta é, em si, uma poderosa ferramenta de stewardship. A decisão conjunta entre laboratório e corpo clínico sobre quais testes oferecer, restringir ou remover é um ato fundamental de governança diagnóstica. Um exemplo prático e de alto impacto é a remoção do alvo de C. difficile de painéis gastrointestinais para evitar o tratamento de colonização, uma intervenção que demonstrou reduzir significativamente o uso inadequado de antimicrobianos sem causar danos aos pacientes (Ref. 9, 10).
- Garantia da Qualidade Analítica: Manter rigorosos processos de controle de qualidade, validação de novos testes e participação em programas de proficiência para assegurar a acurácia dos resultados.
- Comunicação Rápida e Clara: Relatar os resultados de forma clara e interpretável. A comunicação imediata de resultados críticos (ex: hemocultura positiva, bacilos álcool-ácido resistentes em amostra respiratória) é uma responsabilidade não negociável.
- Colaboração com Programas Institucionais: Trabalhar em estreita colaboração com a Comissão de Controle de Infecção Hospitalar (CCIH) e o programa de stewardship de antimicrobianos, fornecendo dados epidemiológicos essenciais, como os perfis de sensibilidade locais (antibiogramas), que são a base para a terapia empírica racional (Ref. 1, 6).
O Impacto das Inovações Tecnológicas na Prática Clínica e no Controle de Infecção
A introdução de tecnologias de diagnóstico rápido (RDTs) revolucionou a capacidade do laboratório de fornecer informações acionáveis em tempo hábil. Duas tecnologias, em particular, exemplificam essa transformação: a espectrometria de massa MALDI-TOF e os painéis sindrômicos moleculares.
Espectrometria de Massa (MALDI-TOF MS)
A tecnologia MALDI-TOF (Matrix-Assisted Laser Desorption/Ionization Time-of-Flight) permite a identificação de bactérias e leveduras a partir de colônias isoladas em minutos, em vez de horas ou dias necessários para os testes bioquímicos tradicionais (Ref. 1). O princípio baseia-se na criação de um perfil proteico único (predominantemente proteínas ribossômicas) para cada microrganismo, que funciona como uma “impressão digital”. Este perfil é então comparado a um vasto banco de dados para identificação precisa, inclusive de patógenos raros ou de difícil identificação (Ref. 16).
O impacto clínico do MALDI-TOF, especialmente em infecções da corrente sanguínea (ICS), é profundo e bem documentado. Estudos demonstram que sua implementação, quando acoplada a um programa de stewardship de antimicrobianos, reduz drasticamente o tempo para resultados e otimiza a terapia:
- Tempo para Identificação (TPI): O tempo médio para identificação do patógeno em hemoculturas positivas pode ser reduzido de mais de 28 horas para aproximadamente 10-11 horas (Ref. 12, 13).
- Tempo para Terapia Antimicrobiana Ótima (TATO): Consequentemente, o tempo para ajustar a terapia empírica para um tratamento direcionado e otimizado diminui significativamente, passando de mais de 36 horas para menos de 20 horas em alguns estudos (Ref. 12, 13, 14, 15).
Painéis Sindrômicos Moleculares
Os painéis sindrômicos multiplex utilizam a tecnologia de Reação em Cadeia da Polimerase (PCR) para detectar simultaneamente múltiplos patógenos (bactérias, vírus, fungos) e, em alguns casos, genes de resistência, a partir de uma única amostra (Ref. 17). Esses painéis estão disponíveis para diversas síndromes, como infecções respiratórias, gastrointestinais, meningoencefalites e infecções da corrente sanguínea.
A principal vantagem é a velocidade e a abrangência, fornecendo um diagnóstico diferencial amplo em cerca de uma hora (Ref. 18). No entanto, essa capacidade traz desafios significativos, como o alto custo e, principalmente, a interpretação dos resultados. A detecção de múltiplos alvos ou de microrganismos que podem ser colonizantes exige um alto grau de discernimento clínico para diferenciar o verdadeiro patógeno de um espectador inocente (bystander) (Ref. 17).
A Sinergia Indispensável: Diagnóstico Rápido e Stewardship
A evidência científica é conclusiva: os benefícios clínicos e financeiros dos RDTs não são uma consequência automática da tecnologia, mas sim o resultado de sua integração com um programa de stewardship de antimicrobianos (ASP) ativo e responsivo (Ref. 19, 22, 23). Sem uma equipe de stewardship para interpretar os resultados rápidos, contatar a equipe assistencial e recomendar ajustes terapêuticos em tempo real, o ganho de tempo no laboratório é perdido na prática clínica.
Quando essa integração ocorre, os resultados são notáveis, como demonstrado em múltiplos estudos sobre infecções da corrente sanguínea.
Tabela 1: Impacto Clínico da Implementação de Diagnósticos Rápidos (RDTs) com Suporte de Stewardship em Infecções da Corrente Sanguínea
| Estudo (Ref.) | Tecnologia de RDT | Redução no Tempo para Terapia Ótima (TATO) | Impacto na Mortalidade | Impacto no Tempo de Internação (LOS) | Impacto Financeiro |
| Bauer K.A. et al. (2014) (Ref. 20, 21) | PCR multiplex | Redução de 89,7h para 32h | Redução de 21% para 8.9% (p=0.01) | Redução de 23,3 para 15,3 dias (p=0.0001) | Redução de ~$26.298 por paciente |
| Itoh Y. et al. (2019) (Ref. 14, 15) | MALDI-TOF MS | Redução de 91,7h para 53,3h (p<0.001) | Menor taxa de falha clínica (14% vs 33,3%, p<0.001) | Não avaliado diretamente, mas associado a menor falha clínica | Menor incidência de eventos adversos (7,5% vs 23,9%) |
| Verroken A. et al. (2016) (Ref. 12, 13) | MALDI-TOF MS | Redução de 36,1h para 17,9h | Não avaliado | Não avaliado | Não avaliado |
| Tsonas A.M. et al. (2017) (Ref. 23) | Meta-análise de RDTs moleculares | Redução significativa no tempo para terapia efetiva | Redução do risco de mortalidade (OR 0,66, p=0.0002) | Redução do tempo de internação em 2,48 dias (p=0.02) | Não avaliado |
Esses dados transformam a aquisição de RDTs de uma despesa laboratorial em um investimento estratégico com retorno clínico e financeiro comprovado, desde que o componente humano do stewardship seja igualmente valorizado e implementado.
Diagnostic Stewardship (DxS): Formalizando a Ponte entre o Laboratório e a Terapêutica
Se o Antimicrobial Stewardship (ASP) se concentra no uso correto do antimicrobiano, o Diagnostic Stewardship (DxS) foca no uso correto do teste diagnóstico. O DxS é definido como um conjunto de intervenções coordenadas e baseadas em evidências, projetadas para garantir que o teste certo seja solicitado para o paciente certo, no momento certo, a fim de orientar a ação clínica correta (Ref. 24, 25).
A Sinergia entre DxS e ASP
DxS e ASP são parceiros essenciais e sinérgicos (Ref. 26, 27). O DxS atua “a montante” (upstream) do processo, garantindo que a informação diagnóstica gerada seja de alta qualidade e clinicamente relevante. O ASP atua “a jusante” (downstream), garantindo que essa informação seja traduzida na melhor decisão terapêutica possível (Ref. 24). Juntos, eles formam um ciclo virtuoso que otimiza todo o processo de manejo de doenças infecciosas.
Intervenções Práticas de Diagnostic Stewardship
As intervenções de DxS são práticas e podem ser implementadas em qualquer instituição. Exemplos incluem:
- Desenvolvimento de Algoritmos: Criar e implementar algoritmos baseados em evidências para orientar a solicitação de testes, como critérios clínicos claros para a coleta de hemoculturas em UTIs, o que demonstrou reduzir significativamente as taxas de coleta sem impactar negativamente os desfechos dos pacientes (Ref. 28).
- Restrição e Testes Confirmatórios: Limitar a solicitação de testes de baixa utilidade ou alto potencial de confusão (ex: culturas de urina em pacientes assintomáticos) e configurar o sistema para realizar testes confirmatórios automaticamente quando necessário.
- Comentários Interpretativos: Adicionar comentários padronizados e informativos aos laudos laboratoriais para guiar a interpretação e a terapêutica. Por exemplo, um laudo de estafilococo sensível à rifampicina pode incluir a nota: “A rifampicina não deve ser usada em monoterapia para evitar o desenvolvimento de resistência” (Ref. 1).
- Educação e Feedback: Fornecer educação contínua e feedback regular aos prescritores sobre as taxas de utilização de testes e a adequação das solicitações.
A Justificativa Regulatória para o DxS
Um dos argumentos mais poderosos para a implementação do DxS é que ele não é apenas uma iniciativa de melhoria da qualidade, mas uma função essencial e, de fato, obrigatória do laboratório clínico. As normas regulatórias e de acreditação laboratorial, como as do Clinical Laboratory Improvement Amendments (CLIA) nos EUA, exigem que os laboratórios garantam a qualidade em todas as fases do teste, incluindo a adequação clínica e a utilidade dos exames que realizam (Ref. 29, 30).
Esta perspectiva muda fundamentalmente a dinâmica. Ela capacita o laboratório a assumir um papel de liderança na governança da utilização de testes, fornecendo uma justificativa robusta para a implementação de políticas de stewardship que poderiam, de outra forma, encontrar resistência. A discussão passa de “Acreditamos que esta é uma maneira melhor de usar as hemoculturas” para “Para cumprir nossos padrões de acreditação e garantir a utilização apropriada de testes, precisamos implementar um processo estruturado para a solicitação de hemoculturas”. Isso confere autoridade e urgência à iniciativa, tornando-a uma questão de conformidade institucional, e não de opinião profissional.
Desafios, Fatores Limitantes e o Caminho a Seguir
Apesar do claro potencial da aliança diagnóstica, a sua implementação plena enfrenta barreiras significativas que precisam ser reconhecidas e abordadas.
- Custos e Recursos: O alto custo de aquisição e manutenção de plataformas moleculares e de MALDI-TOF é um desafio considerável, especialmente para instituições com recursos limitados (Ref. 31). Além disso, a eficácia do modelo depende da disponibilidade de pessoal treinado, como farmacêuticos clínicos com especialização em doenças infecciosas e microbiologistas clínicos, que são recursos escassos (Ref. 18).
- Interpretação de Dados Complexos: A sensibilidade dos testes moleculares pode ser uma faca de dois gumes. A dificuldade em distinguir uma infecção verdadeira de uma colonização ou contaminação é um desafio diário, especialmente com painéis que testam mais de 20 alvos simultaneamente. Sem uma interpretação cuidadosa no contexto clínico completo do paciente, há um risco real de erro diagnóstico e tratamento desnecessário (Ref. 17, 18).
- Fatores de Confusão e Evidências: A avaliação do impacto real das intervenções é complexa. Os estudos podem ser influenciados por variáveis institucionais, como a maturidade pré-existente do programa de stewardship, diferenças nas populações de pacientes e variações nas taxas de resistência locais, o que pode dificultar a generalização dos resultados (Ref. 1, 25).
- Barreiras Culturais e Logísticas: A transição de um modelo de trabalho não integrado para uma cultura verdadeiramente colaborativa requer a superação de inércias institucionais. Desafios como a integração de sistemas de informação do laboratório com o prontuário eletrônico, a criação de fluxos de trabalho eficientes para comunicação em tempo real e a promoção de um diálogo aberto e respeitoso entre diferentes especialidades são essenciais, mas difíceis de alcançar.
Conclusões: Rumo a uma Prática Integrada, Inteligente e Centrada no Paciente
A era da microbiologia clínica como uma caixa-preta que fornece resultados dias após a solicitação chegou ao fim. Estamos imersos em uma nova realidade onde o laboratório é um parceiro estratégico, um nó central na rede de cuidados ao paciente com doença infecciosa. A jornada para combater a resistência antimicrobiana e melhorar os desfechos clínicos não será pavimentada apenas por tecnologias mais rápidas ou novos medicamentos, mas pela aplicação inteligente e integrada dessas ferramentas através de uma “Aliança Diagnóstica” formalizada e profundamente colaborativa.
O caminho a seguir exige um compromisso institucional com a quebra de barreiras inter departamentais e profissionais. Requer que os clínicos vejam o laboratório como uma extensão de sua capacidade diagnóstica e que os microbiologistas se vejam como consultores clínicos essenciais. Exige o investimento não apenas em máquinas, mas nas pessoas e nos processos que conectam a informação à ação.
Conclama-se, portanto, que cada profissional envolvido no controle de infecção hospitalar, cada infectologista, microbiologista, farmacêutico e gestor de saúde se torne um campeão desta aliança em sua instituição. Ao fortalecer a ponte entre o diagnóstico e a terapêutica, não estamos apenas otimizando um processo; estamos redefinindo o padrão de cuidado, protegendo nossos pacientes e preservando a eficácia dos antimicrobianos para as gerações futuras.
A era da microbiologia reativa terminou. O laboratório deixou de ser apenas um prestador de resultados e se tornou parceiro clínico indispensável. A Aliança Diagnóstica demonstra que, quando diagnóstico rápido e stewardship atuam juntos, o impacto é direto: redução de mortalidade, queda no tempo de internação, menor uso inadequado de antibióticos e ganhos financeiros comprovados.
Para CCIHs, infectologistas e gestores hospitalares, investir nessa integração não é opcional: é a única forma de preservar antimicrobianos, otimizar recursos e garantir a segurança do paciente no século XXI .
Referências Bibliográficas
- PATEL, R. The Clinician and the Microbiology Laboratory: Test Ordering, Specimen Collection, and Result Interpretation. In: Bennett, J. E.; Dolin, R.; Blaser, M. J. (Eds.). Mandell, Douglas, and Bennett’s Principles and Practice of Infectious Diseases. 9th ed. Philadelphia, PA: Elsevier, 2020. cap. 16, p. 194-210.
- Resumo: Este capítulo fundamental serve como base para o artigo, detalhando as responsabilidades mútuas entre clínicos e o laboratório de microbiologia, a importância da comunicação e as diretrizes para a coleta de amostras e utilização de tecnologias diagnósticas modernas como o MALDI-TOF.
- MESSACAR, K.; PARKER, S. K.; TODD, J. K.; DOMINGUEZ, S. R. A More Practical, Economical, Clinically Meaningful Approach: a Timeless Call to Action for Diagnostic and Antimicrobial Stewardship. Journal of Clinical Microbiology, v. 55, n. 5, p. 1271-1273, 2017. DOI: 10.1128/jcm.02264-16.
- Resumo: O artigo resgata os princípios de Raymond C. Bartlett, argumentando que os desafios atuais com diagnósticos moleculares rápidos ecoam problemas antigos de utilização de testes, reforçando a necessidade atemporal de stewardship para garantir a relevância clínica e a custo-efetividade.
- ASSISTANT SECRETARY FOR PLANNING AND EVALUATION (ASPE). COVID-19 and the Rise of Antimicrobial Resistance. Washington, D.C.: U.S. Department of Health and Human Services, 2024. Disponível em: https://aspe.hhs.gov/sites/default/files/documents/47d3ae8c64004377877cac7bbaa0ec50/covid-amr-report.pdf.
- Resumo: Este relatório do governo dos EUA detalha como a pandemia de COVID-19 exacerbou a crise de resistência antimicrobiana, destacando a importância de programas de stewardship e controle de infecção para mitigar esses efeitos.
- CCIH.MED.BR. Terapia Antimicrobiana Sem Segredos: Os Princípios que Salvam Vidas e Evitam Resistência. CCIH.med.br, 2024. Disponível em: https://www.ccih.med.br/terapia-antimicrobiana-sem-segredos-os-principios-que-salvam-vidas-e-evitam-resistencia/.
- Resumo: Artigo do site alvo que enfatiza a importância do diagnóstico rápido (PCR, MALDI-TOF) para permitir o início precoce da terapia direcionada, alinhando-se com os objetivos do stewardship de antimicrobianos.
- YUSEF, D.; LÓPEZ-HORTAL, M.; ROCA, I. Rapid Microbiologic Methods for the Diagnosis of Infection and the Detection of Antimicrobial Resistance. Enfermedades Infecciosas y Microbiología Clínica (English ed.), v. 42, n. S1, p. 13-19, 2024. DOI: 10.1016/j.eimce.2024.01.006.
- Resumo: Este artigo de revisão discute o papel crítico dos métodos microbiológicos rápidos, destacando que a interpretação dos resultados depende inteiramente da qualidade da amostra submetida, reforçando a importância da fase pré-analítica.
- KNOTTNERUS, J. A.; BUNTINX, F. Evidence Base Of Clinical Diagnosis: Evaluation Of Diagnostic Procedures. BMJ, v. 324, n. 7335, p. 477-480, 2002. DOI: 10.1136/bmj.324.7335.477.
- Resumo: Embora mais antigo, este artigo clássico estabelece os fundamentos da pesquisa em diagnóstico, apontando que a avaliação de técnicas diagnósticas é menos avançada que a de tratamentos, um problema que o stewardship de diagnóstico busca corrigir.
- ILGES, D. et al. Positive impact of a diagnostic stewardship intervention on syndromic panel ordering practices and inappropriate C. difficile treatment. Infection Control & Hospital Epidemiology, p. 1-6, 2024. DOI: 10.1017/ice.2024.269.
- Resumo: Estudo de intervenção que demonstra o sucesso de uma iniciativa de stewardship de diagnóstico ao remover o alvo de C. difficile de um painel gastrointestinal, resultando na redução de testes e de tratamentos inadequados, sem diagnósticos tardios.
- CCIH.MED.BR. Novas recomendações da OMS para o gerenciamento clínico de COVID-19. CCIH.med.br, 2021. Disponível em: https://www.ccih.med.br/novas-recomendacoes-da-oms-para-o-gerenciamento-clinico-de-covid-19/.
- Resumo: Artigo que, embora focado em COVID-19, ilustra um princípio geral de coleta de amostras: a importância de coletar amostras do trato respiratório inferior quando a suspeita clínica persiste apesar de um resultado negativo do trato superior.
- VERROKEN, A. et al. Clinical Impact of MALDI-TOF MS Identification and Rapid Susceptibility Testing on Adequate Antimicrobial Treatment in Sepsis with Positive Blood Cultures. PLoS One, v. 11, n. 5, p. e0156299, 2016. DOI: 10.1371/journal.pone.0156299.
- Resumo: Estudo que quantifica o impacto do MALDI-TOF em hemoculturas, mostrando uma redução drástica no tempo para identificação (de 28.3h para ~10h) e no tempo para tratamento antimicrobiano ótimo (de 36.1h para ~18h).
- ITOH, Y. et al. Clinical impact of matrix-assisted laser desorption ionization-time of flight mass spectrometry combined with antimicrobial stewardship interventions in patients with bloodstream infections in a Japanese tertiary hospital. Journal of Microbiology, Immunology and Infection, v. 53, n. 2, p. 269-277, 2020. DOI: 10.1016/j.jmii.2019.02.008.
- Resumo: Este estudo prospectivo demonstrou que a combinação de MALDI-TOF com stewardship reduziu significativamente o tempo para terapia efetiva, a taxa de falha clínica e a incidência de eventos adversos em pacientes com infecções da corrente sanguínea.
- SILVA, A. C. B. da; SANTOS, A. C. V. dos; SOUZA, V. M. de. O uso da tecnologia MALDI-TOF MS na identificação de microrganismos de interesse clínico. PIC-Periódico de Iniciação Científica, v. 6, n. 1, p. 28-41, 2022. Disponível em: https://uniceub.emnuvens.com.br/pic/article/view/7624.
- Resumo: Revisão que destaca a capacidade do MALDI-TOF de identificar com precisão microrganismos incomuns diretamente de hemoculturas positivas, acelerando o diagnóstico de patógenos emergentes como Listeria monocytogenes.
- RAMANAN, P. et al. Syndromic Panel-Based Testing in Clinical Microbiology. Clinical Microbiology Reviews, v. 31, n. 1, p. e00024-17, 2018. DOI:(https://doi.org/10.1128/CMR.00024-17).
- Resumo: Uma revisão abrangente sobre painéis sindrômicos, discutindo suas vantagens (rapidez, detecção de múltiplos alvos) e os desafios associados, como custo, estratégias de utilização e a interpretação de resultados complexos.
- SALAVERT-LLETÍ, M. et al. Rapid multiplex molecular syndromic panels for the diagnosis of severe infections in critically ill patients. Medicina Intensiva (English Edition), 2024. DOI: 10.1016/j.medine.2024.07.012.
- Resumo: Revisão recente que aborda o uso de painéis moleculares rápidos em pacientes críticos, destacando a redução no tempo para diagnóstico e tratamento apropriado, mas também as limitações como falsos-positivos e a necessidade de interpretação cuidadosa.
- BAUER, K. A. et al. Integrating rapid diagnostics and antimicrobial stewardship improves outcomes in patients with antibiotic-resistant Gram-negative bacteremia. Clinical Infectious Diseases, v. 59, n. 2, p. 248-255, 2014. DOI: 10.1093/cid/ciu237.
- Resumo: Estudo de alto impacto que demonstrou que a combinação de diagnóstico rápido com um programa de stewardship ativo reduziu significativamente a mortalidade, o tempo de internação e os custos hospitalares em pacientes com bacteremia por Gram-negativos resistentes.
- TAMMA, P. D.; AITKEN, S. L.; BHALODI, A. A.; BERG, S.; BIAS, T. E.; BOGAERTS, P.; CHEN, S.; COSSAR, R.; COOPER, C.; DINGLE, T. C.; FABRE, V.; GOMEZ-SIMMONDS, A.; HSU, J.; KASSAMALI, Z.; KORVICK, J.; KWON, J. H.; LAU, A. F.; LITO, E.; LIVO, C.; LOMBARDI, D. P.; LOWE, T.; MARAOLO, A. E.; MCNULTY, S.; MEYERS, A.; MICALLEF, C.; OLIVEIRA, C. R.; PETTIGREW, M. M.; PIERCE, V. M.; PRANAV, P.; RIVERA, C. G.; SHERWIN, R.; SHUTT, K. A.; SIMNER, P. J.; SMITH, B. A.; SOOKLAL, S.; SUTTON, G.; ZASOWSKI, E. J. Rapid Diagnostic Tests and Antimicrobial Stewardship Programs for the Management of Bloodstream Infection: What Is Their Relative Contribution to Improving Clinical Outcomes? A Systematic Review and Network Meta-analysis. Clinical Infectious Diseases, v. 79, n. 2, p. 502–512, 2024. DOI: 10.1093/cid/ciae166.
- Resumo: Uma meta-análise em rede recente que compara o impacto clínico de diagnósticos rápidos versus culturas convencionais, com e sem programas de stewardship, concluindo que os benefícios são mais pronunciados quando os testes rápidos são integrados a um ASP.
- BRANDA, J. A.; HANSON, K. E. Novel diagnostic stewardship in infectious disease. Drugs in Context, v. 12, p. 1-10, 2023. DOI: 10.7573/dic.2022-11-2.
- Resumo: Artigo que define o stewardship de diagnóstico moderno, descrevendo-o como intervenções que atuam “a montante” e sinergicamente com os esforços tradicionais de stewardship de antimicrobianos para garantir o teste certo para o paciente certo.
- FARON, M. L.; BUCHAN, B. W.; LEDEBOER, N. A. Diagnostic Stewardship in Clinical Microbiology, Essential Partner to Antimicrobial Stewardship. Clinical Chemistry, v. 68, n. 1, p. 60-66, 2022. DOI: 10.1093/clinchem/hvab206.
- Resumo: Este artigo define o stewardship de diagnóstico como um parceiro essencial do stewardship de antimicrobianos, focando em garantir o diagnóstico correto enquanto o ASP otimiza o tratamento, ambos visando melhorar os desfechos do paciente.
- SNYDER, A. et al. Implementation of a diagnostic stewardship intervention to improve blood-culture utilization in 2 surgical ICUs: Time for a blood-culture change. Infection Control & Hospital Epidemiology, v. 44, n. 11, p. 1826-1831, 2023. DOI: 10.1017/ice.2023.28.
- Resumo: Um exemplo prático de stewardship de diagnóstico, onde a implementação de um algoritmo para coleta de hemoculturas em UTIs cirúrgicas levou a uma redução significativa (55-72%) nas taxas de coleta sem aumento de desfechos negativos.
- DIEN BARD, J. et al. The Laboratory’s Essential Role in Diagnostic Stewardship. Journal of Clinical Microbiology, v. 62, n. 11, p. e00552-24, 2024. DOI: 10.1128/jcm.00552-24.
- Resumo: Artigo crucial que argumenta que o stewardship de diagnóstico não é apenas uma boa prática, mas é essencialmente uma exigência imposta pelos requisitos regulatórios e de acreditação laboratorial, capacitando o laboratório a liderar essas iniciativas.
Autor:
Antonio Tadeu Fernandes:
https://www.linkedin.com/in/mba-gest%C3%A3o-ccih-a-tadeu-fernandes-11275529/
https://www.instagram.com/tadeuccih/
#Microbiologia #CCIH #Stewardship #DiagnosticoRapido #SegurancaDoPaciente #InfeccaoHospitalar #Medicina #MALDI_TOF #paineismoleculares #PCR
Instituto CCIH+ Parceria permanente entre você e os melhores professores na sua área de atuação
Conheça nossos cursos de especialização ou MBA:
MBA Gestão em Saúde e Controle de Infecção
MBA Gestão em Centro de Material e Esterilização
MBA EQS – Gestão da Segurança do Paciente e governança clínica
Especialização em Farmácia Clínica e Hospitalar
Pós-graduação em Farmácia Oncológica